INTRODUCCIÓN
Las enfermedades cardiovasculares continúan siendo actualmente la principal causa de morbilidad y mortalidad a nivel mundial. La predicción de eventos cardiovasculares (ECV) es de vital importancia para la identificación temprana de individuos en riesgo y a través de ella la implementación de intervenciones preventivas más apropiadas. (1,2)
Por ese motivo se recomienda estimar el riesgo cardiovascular (RCV) global en todos los pacientes hipertensos para decidir conductas terapéuticas y de control de los factores de riesgo cardiovascular. La información obtenida a partir de la anamnesis, el examen físico, la medición de la presión arterial en el consultorio (PAC) y los resultados de estudios complementarios recomendados, determinan la presencia de factores de riesgo asociados, compromiso o daño de órgano blanco y antecedentes de eventos cardiovasculares. Con esta información es posible estratificar el RCV global del paciente hipertenso y determinar su riesgo como bajo, moderado, alto y muy alto. El conocimiento de la estratificación del RCV global del paciente individual representa una importante información pronóstica, facilita el enfoque global de la prevención y un tratamiento farmacológico adecuado. (3,4)
Una serie de fórmulas o scores de riesgo son propuestos a fin de calcular el RCV. Los calculadores que de ellas surgen constituyen un grupo heterogéneo con diferentes limitaciones (variables cualitativas, estudios complementarios que no se utilizan en la práctica clínica cotidiana) y muchos de ellos sin validación para la población de nuestro país. (3,4,5)
El Consenso Argentino de Hipertensión Arterial propone un enfoque similar al utilizado por la Sociedad Europea de Hipertensión y adaptado para nuestro medio. (5)
Si bien en la actualidad la medición de la presión arterial en el consultorio es el método diagnóstico recomendado, no se encuentra exenta de significativa variabilidad y sesgos por imprecisión en la técnica de medición. Por tal motivo, diferentes guías nacionales e internacionales recomiendan obtener mediciones fuera del consultorio, mediante el monitoreo ambulatorio de presión arterial (MAPA) para confirmar el diagnóstico de hipertensión arterial (HTA) y aportar información pronóstica más precisa. (5,6,7)
En los últimos años, el MAPA se ha convertido en un estudio complementario de gran utilidad para el diagnóstico y evaluación pronóstica de ECV en pacientes hipertensos en comparación con las mediciones aisladas realizadas en el consultorio. Además, el MAPA puede proporcionar datos adicionales, como la variabilidad de la presión arterial, los patrones de descenso nocturno y los valores de presión arterial promedio en diferentes períodos del día. (8-10)
Aunque los modelos de predicción del riesgo cardiovascular han mejorado en precisión a lo largo de los años, todavía existe cierta incertidumbre en las estimaciones. En la actualidad no se consideran las variables hemodinámicas que aporta el MAPA para la estratificación del riesgo cardiovascular en pacientes hipertensos. (11,12)
En este sentido, es importante destacar la necesidad de herramientas más precisas en su capacidad predictiva que incorporen las diferentes variables de presión arterial estudiadas en el MAPA.
Una de las herramientas metodológicas para el análisis predictivo en diferentes áreas de la medicina, más difundidas y en pleno desarrollo en la actualidad son las redes neuronales artificiales (RNA). El análisis con RNA como modelo de inteligencia artificial (IA) ha demostrado superioridad en la precisión pronóstica al compararlas con herramientas estadísticas (en particular cuando existen asociaciones no lineales), que utilizamos habitualmente, como el análisis multivariado y la regresión logística. (13,14,15)
Las RNA pueden detectar características relevantes en los datos y ajustar sus pesos sinápticos y conexiones para mejorar el rendimiento predictivo, que depende entre otras cosas de la cantidad de variables ingresadas y al entrenamiento que reciban, permitiéndoles hacer predicciones más precisas. (16,17,18)
La aplicación de diferentes modelos de máquinas de aprendizaje, ha tenido como objetivo la detección precoz y el tamizaje para identificar a aquellos que desarrollan hipertensión arterial. (19,20,21,22)
El análisis mediante RNA integrando las variables estudiadas en el MAPA podrían mejorar la capacidad predictiva y proporcionar información para diseñar una estratificación del RCV más precisa y completa en comparación con los modelos existentes.
El objetivo de este estudio fue evaluar la capacidad discriminativa de eventos graves en el seguimiento de pacientes hipertensos con el análisis de RNA integrando las variables del MAPA, en comparación con la estratificación de riesgo clínico convencional.
MATERIAL Y MÉTODOS
Se analizó una base de datos con las mediciones registradas en estudios de MAPA con los siguientes criterios de inclusión: pacientes adultos (mayores de 18 años), con diagnóstico de hipertensión arterial esencial con tratamiento farmacológico estudiados con MAPA para evaluar la eficacia terapéutica. Con seguimiento completo a través de la historia clínica informatizada y consultas clínicas de un Hospital de comunidad.
Se incluyeron estudios consecutivos de MAPA realizados entre septiembre de 2013 y abril de 2020 con un seguimiento clínico completo hasta noviembre del 2022. La transferencia de los datos de los informes de los estudios de MAPA (se tuvieron en cuenta los promedios de cada una de las variables analizadas) a una planilla de cálculo y su procesamiento se realizó mediante la aplicación de los programas informáticos Visual Basic y SQL.
Para realizar la estratificación del riesgo cardiovascular se utilizó como modelo las variables propuestas en el Consenso Argentino de Hipertensión Arterial (Sociedad Argentina de Cardiología, Sociedad Argentina de Hipertensión Arterial, Federación Argentina de Cardiología). (5)
Las variables consideradas son las siguientes: a) Factores de riesgo: edad, género, antecedentes de dislipemia, diabetes, tabaquismo, obesidad; b) Compromiso de órgano blanco: diagnóstico de hipertrofia ventricular izquierda (HVI) por ecocardiograma, insuficiencia renal crónica (estadios 1 y 2); c) Condiciones clínicas asociadas o antecedente de eventos cardiovasculares: infarto agudo de miocardio (IAM), insuficiencia cardiaca (IC), accidente cerebrovascular y/o ataque isquémico transitorio (ACV/AIT), enfermedad coronaria, revascularización miocárdica, insuficiencia renal crónica (estadios 3,4 y 5).
Se definió como Bajo riesgo: pacientes con un factor de riesgo asociado; Moderado riesgo: pacientes con dos factores de riesgo asociados; Alto riesgo: pacientes con tres o más factores de riesgo asociados y/o diabetes y/o daño de órgano blanco; Muy alto riesgo: pacientes con antecedentes de eventos cardiovasculares o condiciones clínicas asociadas. (4,5)
Se definió un punto final combinado de eventos serios (ES) en el seguimiento compuesto de la ocurrencia de muerte y/o IAM no fatal y/o ACV y/o AIT y/o IC y/o insuficiencia renal crónica, constatados en la historia clínica informatizada por médicos especialistas en Medicina Interna y Cardiología según las guías nacionales e internacionales vigentes. (3,4,5)
Se desarrollaron modelos de algoritmos de una red neuronal que incluyó a las variables del MAPA como cofactores independientes para su ingreso a la RNA y el de ES como evento dependiente (capa de salida). Un algoritmo NN es un tipo especial de regresión no lineal que presenta múltiples valores mínimos locales. Por lo tanto, cada vez que se ejecute el algoritmo de entrenamiento, convergerá en un modelo diferente. Para elegir el mejor modelo, el proceso de entrenamiento se repitió 50 veces. Sólo se seleccionaron para la comparación los modelos con el mejor poder de discriminación por regresión logística o RNA.
Para los análisis estadísticos y el modelaje de la RNA se usó el programa SPSS 26.0 Statistics. Se compararon diferentes modelos, arquitectura y funciones de activación para seleccionar la de mejor rendimiento en la discriminación del punto final.
Las variables categóricas se expresaron como porcentajes con su IC 95%, mientras que las continuas de acuerdo con su distribución (paramétrica o no paramétrica) como medias y su respectiva desviación estándar o mediana y su rango intercuartílico (RIC) 25-75.
Se evaluó la capacidad discriminativa de la variable dependiente con análisis del área bajo la curva ROC (ABCR) con el análisis del MAPA. Para la comparación de las Áreas Bajo la Curva ROC se utilizó el test de De Long con el programa MEDCALC versión 23.0.9
A fin de identificar las variables con mayor peso y utilidad en el desarrollo de la red neuronal, se realizó un análisis de sensibilidad determinando las importancias normalizadas en el modelo de RNA.
Consideraciones éticas
El estudio fue revisado y aprobado por el Comité de Ética institucional e independiente a esta investigación. Ante la naturaleza observacional del presente análisis no se requirió de consentimiento informado. De acuerdo con la Declaración de Helsinki de la Asociación Médica Mundial, 23 se tomaron todas las precauciones para proteger la privacidad y la confidencialidad de toda la información utilizada.
RESULTADOS
Se analizó en total la información de 491 estudios de MAPA que incluyeron 27 variables numéricas provenientes de cada estudio que se describen a continuación: presión arterial sistólica media de 24 hs (PASm24), presión arterial diastólica media de 24 hs (PADm 24), presión arterial media 24 hs (PAM 24), presión de pulso media de 24 hs (PPm 24), frecuencia cardíaca media de 24 hs (FCm 24), presión arterial sistólica media diurna (PASm Día), presión arterial diastólica media diurna (PADm Día), presión arterial media diurna (PAMm Día), presión de pulso media diurna (PPm Día), frecuencia cardíaca media diurna (FCm Día), presión arterial sistólica media nocturna (PASm Noche), presión arterial diastólica media nocturna (PADm Noche), presión arterial media nocturna (PAMm Noche), presión de pulso media nocturna (PPm Noche), frecuencia cardíaca media nocturna (FCm Noche), variabilidad de la presión arterial sistólica en 24 hs (PASsd 24), variabilidad de la presión arterial diastólica en 24 hs (PADsd 24), variabilidad de la presión de pulso en 24 hs (PPsd 24), variabilidad de la presión arterial media en 24 hs (PAMsd 24), variabilidad de la frecuencia cardíaca en 24 hs (FCsd 24), carga hipertensiva sistólica diurna (Carga HtaSist Día), carga hipertensiva diastólica diurna (Carga HtaDiast Día), carga hipertensiva sistólica nocturna (Carga HtaSist Noche), carga hipertensiva diastólica nocturna (Carga HtaDiast Noche), presión arterial diurna ≥ 135/85 mmHg (HTA diurna), presión arterial nocturna ≥ 120/70 mmHg (HTA nocturna), ritmo circadiano con caída nocturna de PAS y/o PAD < 10% (patrón non dipper).
En la Tabla 1 se detallan los promedios de cada una de las variables de los estudios de MAPA utilizados para el modelaje de las RNA para el punto final combinado.
Tabla 1
Descripción de los valores promedios de las variables analizadas en los estudios de MAPA.
| Variables del MAPA | Valores promedios |
|---|---|
| PASm 24 | 126,16±11,65 mmHg |
| PADm 24 | 79,22 ± 9,30 mmHg |
| PAMm 24 | 94,87 ± 9,4 mmHg |
| FCm 24 | 75,21 ± 8,5 lpm |
| PPm 24 | 46,93 ± 7,62 mmHg |
| PASsd 24 | 17,92 ± 5,6 mmHg |
| PADsd 24 | 14,52 ± 4,2 mmHg |
| PPsd 24 | 16,9 ± 6,1 mmHg |
| PAMsd 24 | 13,51 ± 3,8 mmHg |
| FCsd 24 | 11,59 ± 3,1 lpm |
| PASm Día | 130,13 ± 12,2 mmHg |
| PADm Día | 82,35 ± 9,9 mmHg |
| PAMm Día | 98,17 ± 10,14 mmHg |
| FCm Día | 78,85 ± 9,1 lpm |
| PPm Día | 47,77 ± 8,08 mmHg |
| PASm Noche | 117,34± 13,47 mmHg |
| PADm Noche | 72,23 ± 9,90 mmHg |
| PPmNoche | 48,10 ± 8,99 mmHg |
| PAMm Noche | 87,27 ± 10,50 mmHg |
| FCm Noche | 67,47 ± 9,2 lpm |
| Carga Hta Sist Día | 34,86% |
| Carga Hta Diast Día | 42,25% |
| Carga Hta Sist Noche | 39,47% |
| Carga Hta Diast Noche | 49,68% |
| HTA Noche | 58,4% (IC 95% 55-72) |
| HTA Día | 43,9% (IC 95% 40-56) |
| Non dipper | 42,6% (IC 95% 39-55) |
Carga HtaDiast Día: carga hipertensiva diastólica diurna; Carga HtaDiast Noche: carga hipertensiva diastólica nocturna; Carga HtaSist Día: carga hipertensiva sistólica diurna; Carga HtaSist Noche: carga hipertensiva sistólica nocturna; FCm 24: frecuencia cardíaca media de 24 hs; FCm Día: frecuencia cardíaca media diurna; FCm Noche: frecuencia cardíaca media nocturna; FCsd 24: variabilidad de la frecuencia cardíaca en 24 hs; HTA diurna: presión arterial diurna ≥ 135/85 mmHg; HTA nocturna: presión arterial nocturna ≥120/70 mmHg; MAPA: monitoreo ambulatorio de la presión arterial; Non dipper: ritmo circadiano con caída nocturna de PAS y/o PAD < 10%; PADm 24: presión arterial Diastólica media de 24 hs; PADm Día: Presión Arterial Diastólica media diurna; PADm Noche: Presión Arterial diastólica media nocturna; PADsd 24: variabilidad de la presión arterial diastólica en 24 hs; PAM 24: presión arterial media 24 hs; PAMm Día: presión arterial media diurna; PAMm Noche: presión arterial media nocturna; PAMsd 24: variabilidad de la presión arterial media en 24 hs; PASm 24: presión arterial sistólica media de 24 hs; PASm Día: presión arterial sistólica media diurna; PASm Noche: presión arterial sistólica media nocturna; PASsd 24: variabilidad de la presión arterial sistólica en 24 hs; PPm 24: presión de pulso media de 24 hs; PPm Día: presión de pulso media diurna; PPm Noche: presión de pulso media nocturna; PPsd 24: variabilidad de la presión de pulso en 24 hs.
La edad media de la población fue de 64 ± 14 años, 47% eran mujeres, 12 % tenían diabetes, 11% eran tabaquistas activos, 52% dislipidémicos y el índice de masa corporal promedio fue de 26 ± 4 kg/m2.
La mediana del seguimiento de los pacientes fue de 6,6 años (RIC 4.5-8). La incidencia del punto final en el seguimiento fue 2,6%. En la Tabla 2 se detallan los mejores modelos de RNA con sus funciones de activación neuronales de la capa oculta y de salida y su Área Bajo la Curva ROC.
Tabla 2
Modelos de redes neuronales de mejor rendimiento (perceptrón multicapa con una capa oculta, dos capas ocultas y con modelo de base radial) con sus funciones de activación neuronal de la capa oculta y la capa de salida, la arquitectura neuronal y su área bajo la curva ROC.
| Modelo | Función de activación capa oculta | Función de activación capa de salida | Arquitectura neuronal | Área bajo la curva ROC |
|---|---|---|---|---|
| Perceptrón multicapa con una capa oculta | Hiperbólica tangente | Softmax | 27/7/2 | 0,81 (IC 95% 0,77-0,90) |
| Perceptrón multicapa con dos capas ocultas | Hiperbólica tangente | Softmax | 27/20/15/2 | 0,75 (IC 95% 0,68-0,80) |
| Base radial | Softmax | Identity | 27/6/2 | 0,68 (IC 95% 0,61-0,70) |
| Test de De Long | Perceptrón multicapa 1 capa oculta vs 2 capas ocultas | Perceptrón multicapa 1 capa oculta vs Base radial | Base radial vs Perceptrón multicapa 2 capas ocultas | |
| Valor de p | 0,040 | 0,002 | 0,001 | |
Los modelos de mejor rendimiento fueron el de Perceptrón Multicapa de una capa oculta (función de activación de las neuronas de la capa oculta de tipo hiperbólica tangente) y los de la capa de salida de tipo softmax con una arquitectura neuronal (27/7/2) que describen los nodos de cada una de las capas (Figura 1). En la Tabla 3 se describen los pesos sinápticos con los que se construye y entrena la red neuronal para la predicción del punto final. Se utilizó como función de activación de la capa de entrada la de tangente hiperbólica y la softmax para la capa oculta. Se dividió la muestra con una segmentación de 70% del grupo entrenamiento y 30% de validación de los algoritmos. Se tuvieron en cuenta los pesos o ponderaciones sinápticas estimadas para el desarrollo y testeo de un modelo de perceptrón multicapa para el punto final combinado basados en la entrada de las 27 variables de los estudios de MAPA analizados.
Fig. 1
Arquitectura de la red neuronal del tipo perceptrón multicapa con una capa oculta con 27 neuronas en la capa de entrada, 7 neuronas en la capa oculta y 2 neuronas en la capa de salida.
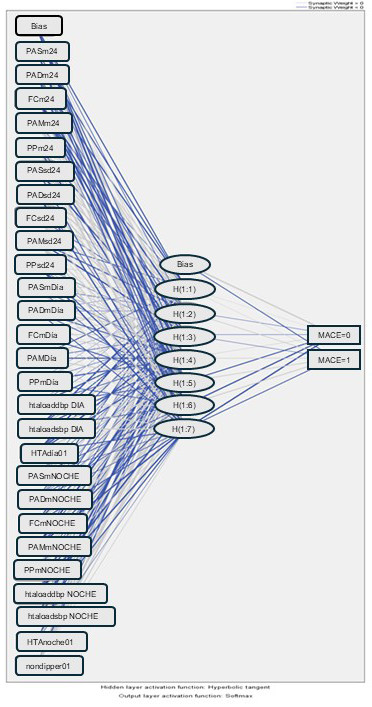
FCm 24: frecuencia cardíaca media de 24 hs; FCm Día: frecuencia cardíaca media diurna; FCm Noche: frecuencia cardíaca media nocturna; FCsd 24: variabilidad de la frecuencia cardíaca en 24 hs; HTA día: presión arterial diurna ≥ 135/85 mmHg; HTA noche: presión arterial nocturna >=120/70 mmHg; htaloaddbp DIA: carga hipertensiva diastólica diurna; htaloaddbp NOCHE: carga hipertensiva diastólica nocturna; htaloadsbp DIA: carga hipertensiva sistólica diurna; htaloadsbp NOCHE: carga hipertensiva sistólica nocturna; Non dipper: ritmo circadiano con caída nocturna de PAS y/o PAD < 10%; PADm 24: presión arterial diastólica media de 24 hs; PADm Día: presión arterial diastólica media diurna; PADm Noche: presión arterial diastólica media nocturna; PADsd 24: variabilidad de la presión arterial diastólica en 24 hs; PAM 24: presión arterial media 24 hs; PAMm Día: presión arterial media diurna; PAMm Noche: presión arterial media nocturna; PAMsd 24: variabilidad de la presión arterial media en 24 hs; PASm 24: presión arterial sistólica media de 24 hs; PASm Día: presión arterial sistólica media diurna; PASm Noche: presión arterial sistólica media nocturna; PASsd 24: variabilidad de la presión arterial sistólica en 24 hs; PPm 24: presión de pulso media de 24 hs; PPm Día: presión de pulso media diurna; PPm Noche: presión de pulso media nocturna; PPsd 24: variabilidad de la presión de pulso en 24 hs.
Tabla 3
Descripción de los pesos sinápticos con los que se construye y entrena la red neuronal para la predicción del punto final.
| Predichos | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Capa oculta 1 | Capa de salida | ||||||||||
| Predictor+A1:L42 | O (1:1) | O (1:2) | O (1:3) | O (1:4) | O (1:5) | O (1:6) | O (1:7) | PF | [PF=0] | [PF=1] | |
| Capa de entrada | (Sesgo) | ,526 | ,579 | -,457 | -,125 | -,394 | -,600 | ,459 | |||
| nondipper 0 | ,560 | ,134 | -,105 | -,501 | -,245 | ,258 | ,314 | ||||
| nondipper 1 | ,293 | -,190 | ,180 | -,293 | -,418 | -,298 | -,112 | ||||
| HTAnoche 0 | -,018 | -,055 | ,410 | -,073 | ,170 | -,531 | ,356 | ||||
| HTAnoche 1 | ,046 | ,100 | -,270 | ,251 | -,128 | -,358 | ,424 | ||||
| HTAdia01 0 | ,209 | -,108 | -,165 | -,299 | ,332 | -,427 | ,505 | ||||
| HTAdia01 1 | ,459 | -,275 | ,110 | ,368 | ,169 | -,669 | ,200 | ||||
| PASm24 | ,119 | -,452 | -,159 | ,315 | ,005 | -,141 | ,388 | ||||
| PADm24 | ,334 | -,166 | ,080 | -,167 | ,241 | ,417 | -,365 | ||||
| FCm24 | ,228 | -,080 | ,435 | -,323 | ,136 | -,457 | ,551 | ||||
| PAMm24 | ,486 | ,475 | ,216 | ,019 | ,036 | -,313 | ,321 | ||||
| PPm24 | -,361 | -,470 | -,308 | -,269 | -,080 | ,020 | -,005 | ||||
| PASsd24 | -,179 | -,346 | -,027 | ,319 | -,312 | ,002 | ,427 | ||||
| PADsd24 | -,275 | ,037 | -,240 | ,050 | -,378 | ,697 | -,199 | ||||
| FCsd24 | -,184 | ,178 | -,381 | ,133 | ,228 | -,230 | -,109 | ||||
| PAMsd24 | -,208 | ,170 | -,290 | ,268 | -,269 | ,153 | -,023 | ||||
| PPsd24 | ,088 | ,233 | -,445 | ,141 | -,167 | ,184 | ,347 | ||||
| PASmDIA | -,089 | -,398 | ,480 | ,291 | ,325 | ,331 | -,216 | ||||
| PADmDIA | -,330 | ,307 | -,107 | ,391 | ,243 | -,350 | ,110 | ||||
| FCmDIA | -,427 | ,294 | -,401 | -,089 | -,330 | -,263 | ,154 | ||||
| PAMmDIA | -,470 | ,010 | ,345 | ,318 | -,147 | -,041 | -,604 | ||||
| PPmDIA | ,053 | ,222 | ,373 | ,179 | ,133 | -,169 | -,001 | ||||
| htaloadsbpDIA | ,476 | ,488 | -,056 | -,249 | ,460 | -,051 | ,265 | ||||
| htaloaddbpDIA | ,265 | ,474 | ,331 | -,092 | ,126 | ,365 | ,372 | ||||
| PASmNOCHE | -,266 | -,077 | -,196 | -,281 | -,514 | ,146 | -,317 | ||||
| PADmNOCHE | ,134 | ,278 | -,099 | ,426 | -,488 | ,554 | ,269 | ||||
| FCmNOCHE | -,429 | -,124 | -,280 | -,184 | ,066 | ,307 | -,257 | ||||
| PAMmNOCHE | -,260 | ,253 | ,435 | ,511 | -,116 | -,308 | -,046 | ||||
| PPmNOCHE | ,313 | -,343 | -,294 | ,278 | -,272 | -,245 | -,196 | ||||
| htaloadsbpNOCHE | -,376 | -,294 | ,233 | -,010 | -,285 | -,195 | -,305 | ||||
| htaloaddbpNOCHE | ,189 | -,134 | -,062 | -,336 | ,122 | -,123 | ,276 | ||||
| Capa oculta 1 | (Bias) | -1,302 | 1,206 | -,093 | |||||||
| O (1:1) | -,348 | ,844 | ,712 | ||||||||
| O (1:2) | -,230 | ,008 | ,005 | ||||||||
| O (1:3) | ,121 | -,058 | -,129 | ||||||||
| O (1:4) | ,158 | -,023 | -,129 | ||||||||
| O (1:5) | -,031 | ,045 | -,504 | ||||||||
| O (1:6) | ,589 | -,891 | -,178 | ||||||||
| O (1:7) | -,553 | ,691 | -,168 | ||||||||
FCm 24: frecuencia cardíaca media de 24 hs; FCm Día: frecuencia cardíaca media diurna; FCm Noche: frecuencia cardíaca media nocturna; FCsd 24: variabilidad de la frecuencia cardíaca en 24 hs; HTA día: presión arterial diurna ≥ 135/85 mmHg; HTA noche: presión arterial nocturna >=120/70 mmHg; htaloaddbp DIA: carga hipertensiva diastólica diurna; htaloaddbp NOCHE: carga hipertensiva diastólica nocturna; htaloadsbp DIA: carga hipertensiva sistólica diurna; htaloadsbp NOCHE: carga hipertensiva sistólica nocturna; Non dipper: ritmo circadiano con caída nocturna de PAS y/o PAD < 10%; PADm 24: presión arterial diastólica media de 24 hs; PADm Día: presión arterial diastólica media diurna; PADm Noche: presión arterial diastólica media nocturna; PADsd 24: variabilidad de la presión arterial diastólica en 24 hs; PAM 24: presión arterial media 24 hs; PAMm Día: presión arterial media diurna; PAMm Noche: presión arterial media nocturna; PAMsd 24: variabilidad de la presión arterial media en 24 hs; PASm 24: presión arterial sistólica media de 24 hs; PASm Día: presión arterial sistólica media diurna; PASm Noche: presión arterial sistólica media nocturna; PASsd 24: variabilidad de la presión arterial sistólica en 24 hs; PPm 24: presión de pulso media de 24 hs; PPm Día: presión de pulso media diurna; PPm Noche: presión de pulso media nocturna; PPsd 24: variabilidad de la presión de pulso en 24 hs.
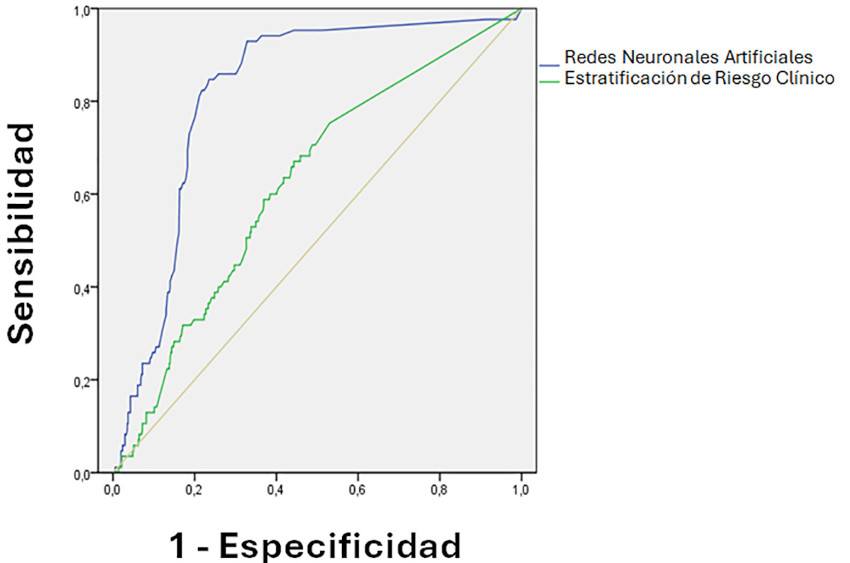
El área bajo la curva ROC del análisis de las variables del MAPA mediante redes neuronales fue 0,81 (IC 95% 0,77-0,90) versus con la estratificación de riesgo clínico 0,67 (IC 95% 0,56-0,77) para el punto final combinado; test de De Long p < 0,001 (Figura 2).
Fig. 2
Comparación de las Áreas Bajo la Curva ROC. Variables del MAPA analizados con redes neuronales artificiales: 0,81 (IC 95% 0,77-0,90) versus estratificación de riesgo clínico 0,67 (IC 95% 0,56-0,77). Test de De Long p < 0,001.
Las variables con mayor peso y utilidad en el desarrollo de la red neuronal o importancias normalizadas en este modelo fueron las siguientes: presión arterial sistólica nocturna (PASm Noche) con un valor del 100%, seguida por la presión arterial sistólica de 24 hs (PASm 24), el IMC, la presión arterial media de 24 hs (PAMm 24), la presión arterial media nocturna (PAMm Noche) y la presión de pulso media de 24 hs (PPm 24) (Figura 3)
Fig. 3
Gráfico de barras representando las variables con mayor importancia normalizada para el desarrollo de la red neuronal artificial en este modelo.
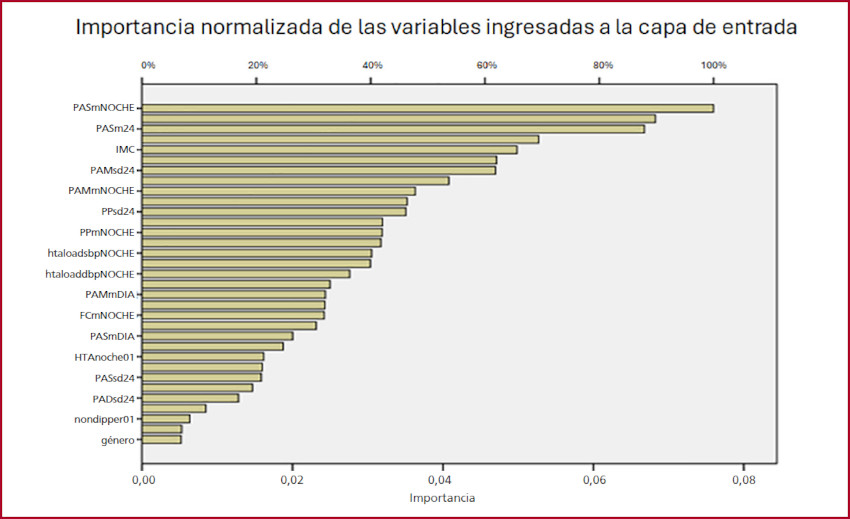
FCm Noche: frecuencia cardíaca media nocturna; HTA noche: presión arterial nocturna ≥120/70 mmHg; htaloaddbp NOCHE: carga hipertensiva diastólica nocturna; htaloadsbp NOCHE: carga hipertensiva sistólica nocturna; IMC: índice de masa corporal; Non dipper: Ritmo circadiano con caída nocturna de PAS y/o PAD < 10%; PADsd 24: variabilidad de la presión arterial diastólica en 24 hs; PAMm Día: presión arterial media diurna; PAMm Noche: presión arterial media nocturna; PAMsd 24: variabilidad de la presión arterial media en 24 hs; PASm 24:presión arterial sistólica media de 24 hs; PASm Día: presión arterial sistólica media diurna; PASm Noche: presión arterial sistólica media nocturna; PASsd 24: variabilidad de la presión arterial sistólica en 24 hs; PPm Noche: presión de pulso media nocturna; PPsd 24: variabilidad de la presión de pulso en 24 hs.
DISCUSIÓN
A nuestro entender, el presente análisis es el primero en reportar la capacidad predictiva de eventos a largo plazo en paciencias hipertensos a través del análisis de las variables de los estudios de MAPA mediante redes neuronales artificiales y su superioridad en comparación con la estratificación de riesgo clínica.
La importancia de estratificar los pacientes hipertensos de acuerdo con el riesgo estimado de presentar un evento cardiovascular permite ajustar el tratamiento en función de dicho riesgo y no solo de las cifras de la PAC. Entre las escalas de riesgo más difundidas están la ecuación de Framingham, el sistema SCORE (Systematic Coronary Risk Evaluation), el QRISK, calculadoras de diferentes sociedades médicas de los Estados Unidos, de la Organización Mundial de la Salud; esta última adaptada para diferentes zonas geográficas. En nuestro país podemos aplicar la estratificación recomendada por el Consenso Argentino de Hipertensión Arterial. (3,4,5)
Sin embargo, los scores tienen varias limitaciones que pueden afectar su precisión y aplicabilidad, entre ellas: las diferencias entre las poblaciones según las regiones geográficas, las características ambientales y socioeconómicas, la subestimación del riesgo en pacientes jóvenes; en muchos casos la diferencia cualitativa de factores de riesgo; la falta de identificación de pacientes con diagnóstico de hipertensión enmascarada. La mayoría de los scores no consideran el tratamiento antihipertensivo en la reducción del riesgo o la predicción de riesgo a corto plazo. (15,16)
A diferencia de la metodología convencional por análisis multivariado, el algoritmo entrenado de la RNA se presenta como herramienta superadora respecto a la capacidad pronóstica de eventos, ya que ingresa todas las variables disponibles en los estudios de MAPA y evita de esta manera un sesgo en la selección de las variables.
Las redes neuronales de tipo Perceptrón Multicapa se encuentran entre las arquitecturas de red más poderosas y populares. Están formadas por una capa de entrada, un número arbitrario de capas ocultas, y una capa de salida. Cada una de las neuronas ocultas o de salida recibe una entrada de las neuronas de la capa previa (conexiones hacia atrás), pero no existen conexiones laterales entre las neuronas dentro de cada capa. La capa de entrada contiene tantas neuronas como categorías correspondan a las variables independientes (categóricas y continuas). La capa de salida corresponde a la variable respuesta, que en este caso es una variable categórica (punto final combinado).
Las redes neuronales de Base Radial son aquellas cuyas funciones de activación en los nodos ocultos son radialmente simétricas. Se dice que una función es radialmente simétrica si su salida depende de la distancia entre un vector que almacena los datos de entrada y un vector de pesos sinápticos, que recibe el nombre de centro o centroide. (17,18,19,20)
Estudios previos aplicando las máquinas de aprendizaje analizaron su utilidad como método de tamizaje y detección precoz de hipertensión en diferentes poblaciones en el mundo, mientras que otros grupos de investigación las aplicaron para la predicción de eventos en pacientes hipertensos. (21,22,24,25,26)
Otros autores han reportado la utilidad de las máquinas de aprendizaje para optimizar la toma de decisiones con el objetivo de mejorar el tratamiento en pacientes hipertensos con base en datos clínicos, logrando una alta precisión al predecir la probabilidad individual de alcanzar los objetivos de la presión arterial en el consultorio con diferentes tratamientos. Las áreas bajo la curva ROC estuvieron muy cerca de 0,90, indicando una elevada precisión de predicción y los coeficientes Kappa resultaron cercanos a 0,8, mostrando elevados niveles de concordancia entre los resultados de objetivos observados y previstos. (27,28)
El área bajo la curva ROC evidencia que las RNA detectan relaciones no lineales entre variables independientes y dependientes más allá del alcance de la regresión logística. Estos resultados respaldan la utilidad de las RNA como una metodología para el análisis en la predicción de eventos graves en pacientes hipertensos. (24,27)
Los modelos de predicción basados en RNA demuestran ser robustos y confiables, podrían implementarse en la práctica clínica como herramientas de apoyo a la toma de decisiones. Esta metodología identificaría de manera temprana a los pacientes hipertensos en mayor riesgo de desarrollar eventos graves y permitiría intervenciones preventivas más efectivas. (22,24,25,26)
Destacamos que la presión arterial sistólica media nocturna (PASm Noche) presentó una importancia normalizada independiente para la determinación del modelo. La presión arterial nocturna ha demostrado ser una variable de riesgo independiente en la predicción de eventos cardiovasculares en pacientes hipertensos, asociada con una mayor incidencia de accidente cerebrovascular, infarto de miocardio, insuficiencia cardíaca e insuficiencia renal. (29)
Durante las horas de la noche, la presión arterial sigue un patrón circadiano característico, con una disminución fisiológica. En pacientes hipertensos, este descenso puede ser insuficiente o incluso invertido, lo que se conoce como non-dipper o reverse-dipper. Estos patrones anormales de presión arterial nocturna se han asociado con un mayor riesgo y eventos cardiovasculares. (29,30,31)
Diferentes publicaciones describieron que el aumento de la PASm Noche se asocia con un mayor riesgo de eventos cardiovasculares en paciente hipertensos, incluso después de ajustar por otros factores de riesgo conocidos. (30,31,32,33,34,35,36,37,38)
Teniendo en cuenta observaciones previas y los resultados obtenidos en el presente estudio mediante el análisis con RNA, podría considerarse a la PASm Noche como un marcador útil en la estratificación del riesgo cardiovascular en pacientes hipertensos. Su evaluación ayudaría a identificar a pacientes con mayor riesgo de complicaciones y permitiría intervenciones clínicas para reducirlos.
La implementación efectiva de los modelos actuales de redes neuronales puede realizarse mediante sistemas de software o hardware. De este modo, los pesos sinápticos de las arquitecturas propuestas, pueden ser entrenados y calculados a través de un algoritmo en Python. A su vez, este algoritmo debe ser capaz de leer automáticamente conjuntos de datos de registros electrónicos de estudios.
Este estudio muestra que el análisis de variables obtenidas en el MAPA mediante el uso de RNA presenta un valor pronóstico significativo para predecir eventos graves en pacientes hipertensos; sugiere la importancia de considerar las variables del MAPA para la estratificación de riesgo en pacientes hipertensos y muestra el uso de las RNA como una herramienta efectiva para el análisis predictivo de eventos cardiovasculares con una adecuada precisión.
Limitaciones
Si bien se utilizaron diversas variables clínicas y las obtenidas en el MAPA, la inclusión de otras mediciones como por ejemplo la microalbuminuria o la enfermedad vascular periférica, podrían proporcionar información adicional para mejorar la capacidad de predicción. La estratificación de riesgo se realizó con todos los datos disponibles en la historia clínica informatizada.
Consideramos que el análisis retrospectivo constituye una limitante por los sesgos concomitantes que inciden en la calidad de la evidencia. Por su carácter de estudio unicéntrico, limitando la transferibilidad de nuestros resultados al mundo real.
Un mayor tamaño de la muestra con un análisis prospectivo, validaciones externas en diferentes cohortes de pacientes hipertensos y la participación de diversos centros asistenciales optimizarían la robustez de esta hipótesis de estudio.
Los algoritmos de las redes neuronales han sido criticados en múltiples oportunidades por ser considerados como una “caja negra” con capacidad limitada para identificar las posibles relaciones causales. En el presente estudio identificamos los factores más influyentes en la modelación del algoritmo, a través de los valores de importancia estandarizada.
La calidad del funcionamiento de las máquinas de aprendizaje y sus algoritmos se asocia a una proporción de eventos mucho mayores que la del presente estudio al igual que con volúmenes de casos de la población total superiores a lo que hemos reportado. Cabe aclarar que la incidencia de eventos registrada en nuestro trabajo es consistente con lo reportado en la literatura en la población de hipertensos ambulatorios. (39,40,41)
CONCLUSIONES
La originalidad de este estudio se basa en ser el primero publicar la capacidad predictiva de las RNA integrando las variables analizadas en los MAPA para predecir eventos a largo plazo en comparación con la estratificación de riesgo cardiovascular recomendada en la actualidad.
Un dato de interés adicional es que observamos que la PAS media nocturna fue variable con mayor ponderación en el funcionamiento de la RNA.
Consideramos este análisis como generador de una hipótesis de investigación a evaluarse con futuros estudios multicéntricos, con una potencia adecuada y con representatividad del mundo real para la transferencia de sus resultados.
Estos algoritmos pueden integrarse al resultado de cada estudio de MAPA, permitiendo calcular automáticamente una probabilidad de riesgo de eventos mayores en el seguimiento de pacientes hipertensos, y así poder colaborar en la toma de decisiones del médico tratante.
Declaración de conflicto de interés
Los autores declaran que no tienen conflicto de intereses.
Agradecimientos
Los autores agradecen al Ingeniero Roberto Bunge (Director de Ingeniería en Inteligencia Artificial de la Universidad San Andrés) y a la Ingeniera Trinidad Monreal (Investigación y Desarrollo del Laboratorio de Inteligencia Artificial y Robótica de la Universidad San Andrés) por sus aportes y conocimientos en inteligencia artificial y redes neuronales.
Financiamiento
Los autores declaran no haber recibido financiamiento alguno para la realización de este trabajo.
Política de uso de la inteligencia artificial
No se utilizaron recursos de inteligencia artificial para la escritura del texto, ni para la generación de tablas ni gráficos.
