INTRODUCCIÓN
La miocardiopatía hipertrófica es un síndrome clínico de origen genético, relativamente frecuente, caracterizado por hipertrofia del ventrículo izquierdo, en ausencia de otra enfermedad cardiaca, sistémica o metabólica que lo justifique. (1) Su origen radica en mutaciones en genes principalmente del sarcómero, y se hereda de forma autosómica dominante en la mayoría de los casos. (2) Presenta un espectro clínico amplio, que va desde pacientes asintomáticos hasta aquellos con insuficiencia cardíaca avanzada o muerte súbita. (3)
Sin embargo, la estratificación pronóstica en MCH continúa siendo un desafío, dada la heterogeneidad en la evolución y la limitada capacidad de los parámetros convencionales para predecir el deterioro de la capacidad funcional. (3-5) El consumo pico de oxígeno (VO2 pico), obtenido mediante prueba de ejercicio cardiopulmonar, constituye un marcador robusto de capacidad funcional y un predictor independiente de morbimortalidad en diversas cardiopatías, incluyendo la MCH. (6) Es así que el VO2 pico fue propuesto como el punto final primario de los principales estudios realizados en esta entidad. (7-9) Sin embargo, las variables clínicas y de imagen que determinan un menor VO2 pico en esta población no están claramente definidas.
La resonancia magnética cardiaca (RMC) se ha consolidado como el estándar de referencia para la evaluación morfológica y funcional del ventrículo izquierdo, permitiendo además la cuantificación precisa de fibrosis mediante realce tardío con gadolinio (RTG). (1,2) Recientemente, la incorporación del análisis del strain longitudinal global por resonancia magnética cardíaca (SLG-RMC) a través de la técnica de feature tracking nos permite detectar estadios más tempranos de compromiso ventricular, no evidenciables con las técnicas convencionales como la medición de fracción de eyección ventricular izquierda (FEVI) mediante volumetría. (10,11) Cabe destacar que en este estudio se utilizó el strain longitudinal global por ser el parámetro más reproducible y el más ampliamente utilizado en la práctica clínica, con menor variabilidad que el strain radial o circunferencial. (12,13)
No obstante, el valor pronóstico de este parámetro en relación con la capacidad funcional en MCH aún requiere mayor evidencia. (14-17)
OBJETIVOS
Evaluamos la asociación entre SLG-RMC y otras variables clínicas, ecocardiográficas y de RMC con el VO2 pico medido en la prueba cardiopulmonar de ejercicio en una cohorte contemporánea de pacientes con diagnóstico confirmado de MCH, con el objetivo de identificar predictores independientes de limitación funcional, que permitan optimizar la estratificación pronóstica en este grupo de pacientes.
MATERIAL Y MÉTODOS
Se realizó un estudio de cohorte retrospectivo, observacional y unicéntrico que incluyó pacientes pertenecientes a un registro institucional de MCH, entre enero de 2017 y marzo de 2025. Todos los pacientes otorgaron consentimiento informado previo a su incorporación al mismo. Los datos para el presente análisis se obtuvieron a partir de la revisión de la historia clínica electrónica institucional.
La MCH se definió como la presencia de aumento de espesores en cualquier segmento del ventrículo izquierdo >15 mm, o >13 mm en familiares de primer grado con diagnóstico de la patología, en ausencia de otra causa que lo justificara. (1) Cuando fue posible, se realizaron estudios genéticos para confirmar la etiología sarcomérica. Se incluyeron pacientes con diagnóstico confirmado de MCH sarcomérica mayores de 18 años y se excluyeron fenocopias u otras causas de hipertrofia ventricular.
Para este trabajo, se seleccionaron únicamente aquellos pacientes que contaban con ecocardiograma, RMC y prueba cardiopulmonar de ejercicio realizados en un intervalo menor o igual a 12 meses entre sí.
Se recolectaron variables demográficas (edad, sexo, altura), clínicas (clase funcional NYHA, tratamiento recibido), ecocardiográficas (FEVI, gradiente intraventricular máximo, presencia de MCH obstructiva definida por gradiente ≥ 30 mmHg en reposo y/o movimiento anterior sistólico de la valva anterior mitral) y parámetros derivados de la RMC (volúmenes y masa ventriculares indexados, FEVI y fracción de eyección del ventrículo derecho, espesor parietal máximo, presencia y cuantificación de RTG, y SLG-RMC del ventrículo izquierdo).
Las RMC se realizaron en un equipo de 1.5 T (Avanto, Siemens Medical Solutions®, Erlangen, Alemania). La cuantificación de RTG (con técnica de 5 umbrales) y el SLG-RMC se efectuaron con el software Circle Cardiovascular Imaging (Tissue Tracking, cvi42, Figura 1). El VO2 pico se determinó mediante la prueba cardiopulmonar en cicloergómetro con protocolo incremental, expresándose en mL/kg/min.
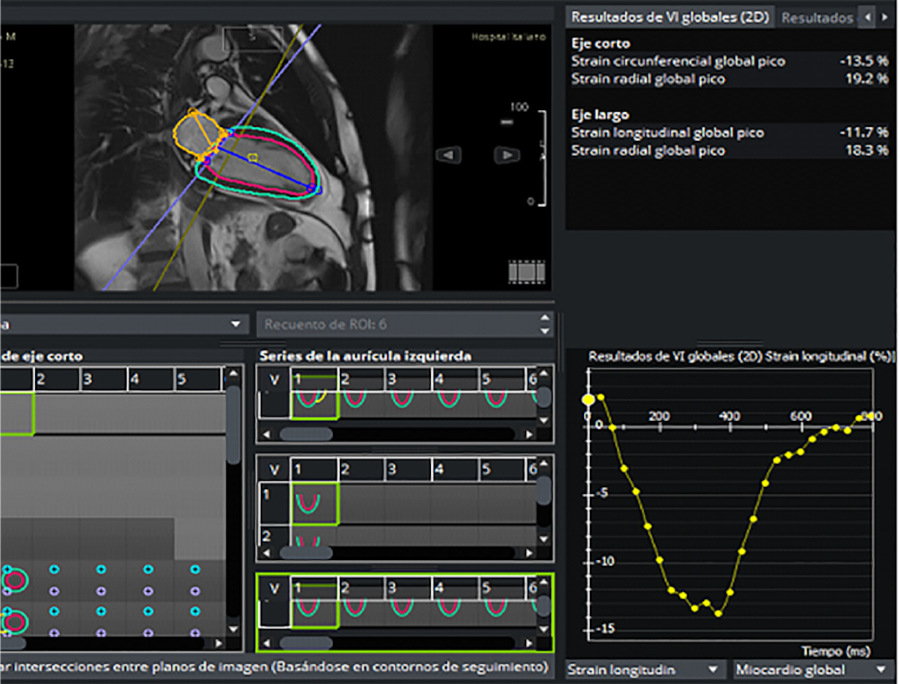
Fig. 1
Ejemplo de análisis de strain longitudinal global del ventrículo izquierdo mediante Circle Cardiovascular Imaging (Tissue Tracking, cvi42)
Análisis estadístico
Las variables continuas se expresaron como media ± desviación estándar (DE) o como mediana y rango intercuartílico (RIC), según su distribución evaluada mediante la prueba de Shapiro-Wilk. Para la comparación entre grupos, se utilizó la prueba t de Student o el test de Mann-Whitney, de acuerdo con la distribución de los datos. Las variables categóricas se presentaron como frecuencias absolutas y porcentajes, y se compararon mediante prueba de Chi² o test exacto de Fisher, según correspondiera.
Con el objetivo de explorar las asociaciones entre las variables clínicas, ecocardiográficas y de RMC con el VO2 pico, se aplicaron modelos de regresión lineal. En el análisis univariado, cada predictor fue evaluado individualmente para identificar correlaciones significativas con el VO2 pico. Posteriormente, aquellas variables con significación estadística (p <0,05) o relevancia clínica se incorporaron a un modelo de regresión lineal multivariado, con el fin de identificar predictores independientes de menor VO2 pico.
Todos los análisis estadísticos se realizaron con el software STATA versión 13.1 (StataCorp LP, College Station, TX, USA), considerando estadísticamente significativos los valores de p <0.05.
Consideraciones éticas
El protocolo del estudio sigue las pautas éticas de la Declaración de Helsinki de 1975 (18) y el diseño del registro institucional de miocardiopatía hipertrófica de donde se obtuvieron los datos, fue aprobado por el comité de ética de nuestra institución.
RESULTADOS
Se incluyó un total de 54 pacientes con diagnóstico de MCH sarcomérica. La edad media fue de 53 ± 18 años, y el 59,2% (n=32) era de sexo masculino. La forma obstructiva de la enfermedad se registró en 26 pacientes (48,1%). El VO2 pico promedio en la población fue de 23,5 ± 9,6 ml/kg/min.
Parámetros de resonancia magnética cardiaca
La FEVI promedio fue 72 ± 10%. La media de espesor parietal máximo fue de 17 ± 4 mm. El RTG estuvo presente en el 94,4% (n=51) de los pacientes, con una masa mediana de 15 gramos y RIC 6,84-33,59 (no se discriminó según porcentaje de RTG). La media de SLG-RMC del VI fue de -13 ± 3,3%. En la Figura 1 se muestra un ejemplo de medición de SLG-RMC en uno de los pacientes de la cohorte. El resto de las variables clínicas, ecocardiográficas, de RMC y de la prueba cardiopulmonar de ejercicio se detallan en la Tabla 1.
Tabla 1
Características generales de la población
| Variables clínicas | |
|---|---|
| Edad al diagnóstico, años, media ± DE | 53 ± 18 |
| Sexo masculino, n (%) | 32 (59,3) |
| Altura, centímetros, media ± DE | 161 ± 33 |
| Clase funcional NYHA* ≥ 2, n (%) | 16 (29,6) |
| IMC*, kg/m2, media ± DE | 28,4 ± 5,1 |
| Hipertensión arterial, n (%) | 21 (38,9) |
| Diabetes mellitus, n (%) | 6 (11,1) |
| Fibrilación auricular, n (%) | 7 (13,0) |
| Disnea, n (%) | 31 (57,4) |
| Angina, n (%) | 12 (22,2) |
| Betabloqueantes, n (%) | 38 (70,4) |
| Calcioantagonistas, n (%) | 7 (13,0) |
| Inhibidores miosina, n (%) | 3 (5,6) |
| CDI*, n (%) | 6 (11,1) |
| Mictomía septal, n (%) | 3 (5,6) |
| Alcoholización septal, n (%) | 2 (3,7) |
| Variables ecocardiograma | |
| Espesor parietal, mm, media ± DE | 17,4 ± 3,9 |
| Diámetro anteroposterior aurícula izquierda, mm, mediana (RIC) | 42 [38-46] |
| Gradiente intraventricular, mmHg, mediana (RIC) | 30 [6-58] |
| SAM, n (%) | 25 (46,3) |
| OTSVI, n (%) | 32 (59,3) |
| Variables resonancia cardiaca | |
| FEVI, %, media ± DE | 72 ± 10 |
| Volumen fin de diástole VI indexado, mL/m2, media ± DE | 72 ± 18 |
| Volumen fin de sístole del VI indexado, mL/m2, mediana (RIC) | 69 [60-78] |
| Máximo espesor, mm, media ± DE | 17 ± 4 |
| Presencia de RTG, n (%) | 51 (94,4) |
| Masa de RTG, gramos, mediana (RIC) | 15 [6.84-33.59] |
| SLG ventrículo izquierdo, %, media ± DE | -13 ± 3,3 |
| Fracción eyección ventrículo derecho, %, media ± DE | 66 ± 7 |
| Volumen fin de diástole VD, mL, media ± DE | 71 ± 15 |
| Volumen de fin de sístole del VD, mL, media ± DE | 27 ± 24 |
| Masa del VI, gramos | 86 ± 24 |
| Variables consumo de oxígeno | |
| VO2 pico (mL/kg/min), media ± DE | 23,5 ± 9,6 |
| VO2 (% del predicho), media ± DE | 83,3 ± 19,5 |
| Frecuencia cardiaca al VO2 pico (lpm), media ± DE | 133,7 ± 30,7 |
| OUES, [(mL/min)/log10], media ± DE | 2156,8 ± 954,7 |
CDI: cardiodesfibrilador implantable; DE: desviación estándar; IMC: índice de masa corporal; FEVI: fracción de eyección del ventrículo izquierdo; NYHA: New York Heart Association; OTSVI: obstrucción al tracto de salida del ventrículo izquierdo; OUES: Oxygen Uptake Efficiency Slope (pendiente de la eficiencia del consumo de oxígeno); RIC: rango intercuartílico; RTG: realce tardío de gadolinio; SAM: movimiento anterior sistólico de la valva anterior mitral; VD: ventrículo derecho; VI: ventrículo izquierdo
Análisis univariado
En el modelo de regresión lineal univariado, se observaron asociaciones significativas entre el VO2 pico y la edad al momento del diagnóstico (β = -0,35; IC 95%: -0,46 a -0,24; p < 0,001), el sexo masculino (β = +8,26; IC 95% +3,37 a +13,14; p = 0,001), el volumen telediastólico indexado del ventrículo derecho (β = +0,31; IC 95% +0,15 a +0,46; p < 0,001) y con el SLG-RMC del VI (β = -0,85; IC 95% -1,62 a -0,08; p = 0,034). No se encontraron asociaciones significativas con la clase funcional NYHA, la presencia de obstrucción dinámica intraventricular, el gradiente intraventricular máximo, la FEVI, los volúmenes ventriculares izquierdos, la masa del VI, el espesor parietal máximo ni con el RTG. En la Tabla 2 se detallan las variables incluidas en el análisis univariado, y su relación con el VO2 pico.
Tabla 2
Modelo de regresión lineal univariado
| Variable | Regresión lineal univariada | p valor |
|---|---|---|
| Coeficiente β (IC 95%) | ||
| Edad al diagnóstico | -0,35 (-0,46 a -0,24) | <0,001 |
| Sexo masculino | +8,26 (+3,37 a +13,14) | 0,001 |
| Disnea NYHA | -2,59 (-5,35 a +0,17) | 0,065 |
| Gradiente máximo intraventricular (mmHg) | -0,06 (-0,15 a +0,02) | 0,110 |
| MCH obstructiva | -1,14 (-6,44 a +4,17) | 0,669 |
| FEVI % | +0,11 (-0,16 a +0,38) | 0,425 |
| Volumen fin diástole VI indexado (ml/m²) | +0,08 (-0,06 a +0,23) | 0,265 |
| Volumen fin de sístole del VI indexado (ml/m²) | -0,05 (-0,15 a +0,05) | 0,320 |
| Masa ventricular izquierda (g/m²) | -0,0007 (-0,11 a +0,11) | 0,921 |
| Espesor parietal máximo (mm) | +0,09 (-0,60 a +0,79) | 0,781 |
| RTG cuantitativo (%) | -0,004 (-0,10 a +0,09) | 0,934 |
| RTG (presente) | +2,35 (-18 a 23,2) | 0,821 |
| FEVD (%) | +0,25 (-0,10 a +0,60) | 0,162 |
| Volumen fin de diástole del VD, indexado (ml/m²) | +0,31 (+0,15 a +0,46) | <0,001 |
| Volumen fin de sístole del VD, indexado (ml/m²) | -0,018 (-0,13 a +0,09) | 0,743 |
| Strain RMN (%) | -0,85 (-1,6 a -0,08) | 0,034 |
FEVD: fracción de eyección del ventrículo derecho; FEVI: fracción de eyección del VI; MCH: miocardiopatía hipertrófica; NYHA: New York Heart Association; RMC: resonancia magnética cardíaca; RTG: realce tardío de gadolinio; VD: ventrículo derecho; VI: ventrículo izquierdo.
Análisis multivariado
En el modelo de regresión lineal multivariado (Tabla 3), los predictores independientes de menor VO2 pico fueron: el sexo femenino (β = -6,1; IC 95% - 10,56 a -1,75; p=0,007), una mayor edad al momento del diagnóstico (β = -0,26 ; IC 95%: -0.37 a -0,15; p<0,001) y un menor SLG-RMC del VI (β = -0,59, IC 95%: -1,14 a -0,04; p= 0,033).
DISCUSIÓN
En esta cohorte contemporánea de pacientes con MCH, observamos que un menor valor de SLG-RMC del VI se asoció de forma independiente con una menor capacidad funcional, medida por el VO2 pico en la prueba cardiopulmonar de ejercicio. Este hallazgo podría aportar una perspectiva fisiopatológica relevante, con la hipótesis de que la limitación funcional en la MCH no dependería sólo del grado de hipertrofia ni de la presencia de obstrucción dinámica, sino también de una insuficiencia contráctil miocárdica tanto clínica como subclínica, detectable por SLG-RMC, incluso en pacientes con FEVI conservada. El SLG, al reflejar la capacidad de deformación longitudinal del miocardio, constituye un marcador sensible de la eficiencia contráctil y permite detectar disfunción mecánica temprana antes de que se manifiesten alteraciones globales de la FEVI o síntomas avanzados. (19,20) Es destacable que todos los pacientes de nuestra cohorte presentaron FEVI preservada.
La alteración del SLG probablemente representa la expresión funcional de los mecanismos moleculares propios de la MCH, caracterizados por una pérdida progresiva de eficiencia contráctil, que se traduce en menor acortamiento miocárdico y, en consecuencia, en una capacidad limitada para incrementar el gasto cardíaco durante el esfuerzo. Es decir, un SLG reducido implica una menor reserva contráctil y, por lo tanto, una limitación para sostener el gasto cardíaco, lo que se traduce en una disminución del VO2 pico. (14,19) Este fenómeno podría explicar la asociación entre una mayor alteración del SLG-RMC y menor VO2 pico observada en nuestro trabajo, en concordancia con lo descrito en el estudio STRAIN-HCM, donde el SLG se comportó como predictor independiente de eventos adversos. (14,21)
Por otro lado, no encontramos correlación entre el VO2 pico y el monto de fibrosis miocárdica medida por RTG, hallazgo que refuerza la idea de que el SLG identifica un estadio funcional más precoz del daño miocárdico. (22,23) Cabe destacar que en nuestra cohorte casi todos los pacientes presentaban algún grado de RTG, lo cual sugiere que el valor pronóstico diferencial del SLG no depende exclusivamente de la presencia o ausencia de fibrosis, sino del grado de disfunción mecánica subyacente.
La menor capacidad funcional observada en mujeres en este estudio coincide con lo reportado en otras series, donde el sexo femenino se asocia con fenotipos más sintomáticos, cavidades ventriculares de menor tamaño y mayor predisposición a la obstrucción dinámica. (24) Estos rasgos anatómicos, sumados a un diagnóstico frecuentemente más tardío, podrían explicar en parte la brecha funcional observada. Del mismo modo, la edad más avanzada se comportó como un determinante negativo del VO2 pico, probablemente reflejando el impacto acumulativo de la fibrosis difusa, la rigidez miocárdica y las comorbilidades asociadas. (25,26)
Desde una perspectiva clínica, la incorporación del SLG-RMC en la evaluación de la MCH puede aportar valor pronóstico adicional y permitir una caracterización más precisa del fenotipo funcional. En pacientes con FEVI preservada, una reducción significativa del SLG podría anticipar el deterioro clínico y guiar intervenciones tempranas. Esta aproximación integrada se alinea con la tendencia actual de las guías internacionales AHA/ACC, (1) que promueven una estratificación fisiopatológica y personalizada, superando el enfoque puramente morfológico.
Probablemente, en un futuro, sea necesario desarrollar modelos pronósticos que integren variables clínicas, de imagen y funcionales para refinar la predicción del riesgo en esta población.
Si bien este trabajo presenta limitaciones inherentes a su diseño retrospectivo y a la naturaleza unicéntrica de la muestra, la disponibilidad de estudios complementarios de alta calidad –ecocardiograma, RMC y prueba cardiopulmonar– refuerza la solidez de los resultados. Por otro lado, nuestra población representa un perfil clínico característico de la MCH, con presencia de formas obstructivas, lo cual refuerza la representatividad del grupo y la aplicabilidad de los hallazgos. En conjunto, nuestros datos consolidan la noción de que la MCH es esencialmente una enfermedad de la mecánica miocárdica más que de la hipertrofia per se, y posicionan al SLG-RMC como un marcador potencialmente importante para comprender, cuantificar y seguir la eficiencia contráctil en la práctica clínica.
CONCLUSIONES
En esta cohorte contemporánea de pacientes con MCH, el sexo femenino, la mayor edad y la reducción del SLG-RMC se asociaron de manera independiente con menor VO2 pico.
Estos resultados subrayan la utilidad del SLG-RMC como herramienta complementaria para la estratificación pronóstica y la evaluación funcional, más allá de parámetros convencionales como la FEVI o el RTG. Su implementación sistemática podría optimizar la identificación temprana de pacientes con mayor riesgo de deterioro funcional.
LIMITACIONES
Se mencionan como limitaciones de este trabajo su carácter retrospectivo, así como la falta de estratificación del VO2 pico según el sexo del paciente. A su vez, resulta importante destacar que no se realizó la comparación entre el strain medido por resonancia magnética cardíaca y el strain evaluado mediante ecocardiografía.
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses. (Véanse formularios de conflicto de intereses de los autores en la Web)
Agradecimientos
A todo el servicio de cardiología del Hospital Italiano de Buenos Aires.
Fuentes de financiamiento
Ninguna.
