“Lo esencial puede ser invisible al microscopio”
INTRODUCCIÓN
El trasplante cardíaco es aceptado como la mejor opción terapéutica para los pacientes con enfermedad cardíaca terminal.
El rechazo del injerto, junto con las infecciones, son las complicaciones más frecuentes durante el primer año luego del procedimiento, y dado que el rechazo puede suponer la pérdida del injerto, es de suma importancia poder detectarlo a tiempo para instaurar en forma precoz el tratamiento adecuado. (1)
En el año 2021 se publicó un estudio observacional y retrospectivo llevado a cabo en nuestro país donde se observa, en forma coincidente con la información internacional, que la principal causa de hospitalización durante el primer año postrasplante, fue el rechazo agudo, y dentro de este, el de origen celular. (2)
Las manifestaciones del rechazo agudo abarcan un amplio espectro de presentaciones, que pueden ir desde el deterioro hemodinámico hasta alteraciones genéticas, cada una con diferentes posibilidades diagnósticas. (3) (Figura 1)
Fig. 1
Métodos diagnósticos del rechazo agudo de trasplante según el espectro de presentación.
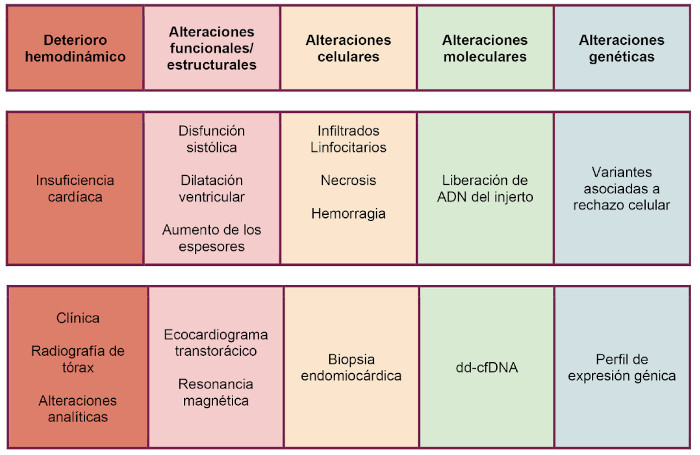
ADN: ácido desoxirribonucleico; dd-cfDNA: ADN libre del donante
El deterioro hemodinámico del paciente se puede detectar clínicamente, lo más habitual como insuficiencia cardíaca, y su diagnóstico puede realizarse mediante una adecuada anamnesis y examen físico, así como con estudios complementarios sencillos, como análisis de laboratorio y radiografía de tórax.
Las alteraciones estructurales y/o funcionales pueden ser identificadas mediante estudios de imágenes. El ecocardiograma y la resonancia magnética son capaces de detectar aumento de espesores, falla diastólica, dilatación ventricular y disfunción sistólica, que pueden ser indicativos de rechazo, pero, lamentablemente, en una etapa más avanzada que la deseada, pues el objetivo es adelantarse al daño estructural del órgano e instaurar precozmente el tratamiento. (4,5,6,7,8,9)
Por este motivo se ha impuesto como estudio rutinario la realización de la biopsia endomiocárdica (BEM), que puede revelar a nivel microscópico distintos grados de infiltrado celular, necrosis y/o hemorragia, los cuales son indicadores de rechazo y además permiten clasificar la gravedad del mismo y guiar el tratamiento.
En el ámbito molecular, la liberación de ácido desoxirribonucleico (ADN) derivado del injerto, mediante la cuantificación del porcentaje del ADN libre de células derivado del donante (dd-cfDNA, por su sigla en inglés) es una opción diagnóstica para identificar el rechazo.
Finalmente, a nivel genético, se han identificado variantes asociadas a rechazo. El perfil de expresión génica (PEG) permite identificar pacientes con mayor riesgo de rechazo.
Dentro del espectro clínico-genético, a medida que más nos acercamos a la instancia molecular, existe la posibilidad de detectar con mayor precocidad el evento. (10,11,12)
PLANTEO DEL PROBLEMA
La técnica más utilizada y costo/efectiva para el diagnóstico y seguimiento del rechazo es la BEM, que posee una adecuada sensibilidad y especificidad para el diagnóstico de rechazo celular, pero cuenta con ciertas limitaciones, entre las cuales se encuentran su invasividad, las complicaciones, la posibilidad de discordancia para calificar los grados intermedios de rechazo celular y la dificultad en la interpretación del rechazo mediado por anticuerpos.
Dentro de las complicaciones de la BEM, debe mencionarse el taponamiento cardíaco, que es poco frecuente (<0,5 %), y la posibilidad de provocar insuficiencia tricuspídea. (13,14)
Un elemento a tener en cuenta es que la terapia inmunosupresora actual ha disminuido la incidencia del rechazo agudo y hay que considerar, además, que la mayoría de los controles rutinarios con BEM se realizan en pacientes asintomáticos y con menor probabilidad de tener rechazo, lo que lleva a una disminución del rendimiento diagnóstico de la técnica. (15)
En las últimas décadas se observó una reducción en la incidencia de rechazo en todos los intervalos post trasplante. En un estudio observacional comparativo entre dos grupos de trasplantados, los de la década de 1990 versus los de la década de 2000, se observó que los últimos tenían más factores de riesgo para desarrollar rechazo, pese a lo cual su incidencia fue menor en el grupo más reciente en todos los intervalos postrasplante analizados (0-6 meses: 60,2 % vs 21,5 %, p < 0,001; 6-12 meses: 26,8 % vs 1,8 %, p < 0,001; 12-36 meses: 32,3 % vs 10,5 %, p=0,006).(16)
La disminución en la incidencia del rechazo, sobre todo después del sexto mes, hace que la probabilidad de detectarlo con la BEM sea muy baja en asintomáticos. Se puede concluir que durante las primeras etapas postrasplante cardíaco el rechazo es la principal causa de hospitalización y mortalidad, y que el método actualmente utilizado para su diagnóstico es invasivo, no se encuentra exento de complicaciones y después de los 6 meses disminuye su rédito diagnóstico en asintomáticos, que son la mayor parte de los pacientes, por lo que se considera necesaria la aplicación de nuevas estrategias que mejoren dicha perspectiva.
Los métodos en los cuales centraremos este artículo, se corresponden con la detección de alteraciones moleculares y genéticas, más allá del alcance del microscopio.
TÉCNICAS DE DIAGNÓSTICO A NIVEL MOLECULAR Y GENÉTICO
ADN circulante del donante (dd-cfDNA)
En condiciones normales, el recambio celular, que ocurre continuamente en los distintos tejidos, provoca presencia de ADN libre circulante en el torrente sanguíneo. El fundamento de esta técnica se basa en la liberación de material genético del donante en la sangre del receptor. Por lo tanto, la posibilidad de detectar y cuantificar dicho material podría encender alarmas en el seguimiento de estos pacientes. Se acepta que el rechazo provoca la liberación de mayores cantidades de ADN del donante, aumentando sus niveles en sangre del receptor. El dd-cfDNA se expresa como el porcentaje del ADN del donante del total del ADN libre en la muestra analizada. Se ha generalizado el término de biopsia líquida para definir el método.
Un estudio comparativo con la BEM estableció el valor normal del dd-cfDNA y su correlación con el grado histológico de rechazo. Aquí también se evidenció que el ascenso del porcentaje de dd-cfDNA es previo a la evidencia histológica de rechazo. (17)
El grupo de investigación D-OAR (Donor-Derived Cell-Free DNA-Outcomes AlloMap Registry ), en 2018, estableció que el dd-cfDNA posee mayor valor predictivo negativo (VPN) que la BEM luego del día 55 post trasplante. (18)
La alianza GRAfT (Genomic Research Alliance for Transplantation ) en un estudio observacional incluyó 171 pacientes trasplantados controlados con BEM y dd-cfDNA. Se constató que un 80% de los pacientes con dd-cfDNA compatible con rechazo (valor >0,25%), no habían sido detectados por la BEM y la gran mayoría desarrollaron rechazo con expresión clínica en el seguimiento. (19,20)
El estudio DEDUCE mostró que luego del segundo año de seguimiento, el dd-cfDNA aumenta progresivamente y podría corresponderse con el desarrollo de vasculopatía del injerto, tornando menos sensible el diagnóstico de rechazo agudo. (21)
Los pacientes con rechazo celular de mayor grado presentan mayor porcentaje de ADN libre. El rechazo mediado por anticuerpos también presenta mayores niveles de ADN libre cuanto mayor es el grado de rechazo; habitualmente son valores más elevados que en el rechazo celular, y con composición aminoacídica distinta.
Un aspecto común a todos los estudios es que esta técnica tiene un alto VPN, alrededor de 97-99 %, y que permitió disminuir el número de BEM, que solo se llevaron a cabo con porcentajes elevados de dd-cfDNA, con el fin de confirmar el rechazo y categorizar su gravedad. En conclusión, este método podría ser utilizado luego de la etapa inicial del trasplante, a partir del 2do o 3er mes postrasplante; permite principalmente descartar, por su alto VPN, tanto el rechazo celular como el mediado por anticuerpos, incluso en forma más temprana que la BEM, y se asocia a un menor uso rutinario de la misma. (22,23,24,25,26)
Perfil de expresión génica (PEG)
El modo en el cual se expresan nuestros genes determina el fenotipo de funciones de todas las células, entre ellas la función inmunológica.
La expresión de algunos genes linfocitarios se asocia con mayor respuesta inmune y mayor posibilidad de rechazo celular.
Las pruebas comerciales más utilizadas detectan la presencia de 11 genes vinculados con rechazo, estableciéndose un puntaje de riesgo según su perfil de activación.
Algunos de los genes implicados son CD3E (activación linfocitaria) y NKG7 (citotoxicidad), entre otros. (27)
Un estudio prospectivo de la Sociedad Internacional de Trasplante de Corazón y Pulmón (ISHLT) observó que los trasplantados con más de 55 días del implante y con un puntaje bajo de PEG no presentaron rechazo con compromiso hemodinámico, muerte ni retrasplante, validando así su uso en poblaciones de bajo riesgo inmunológico.Esta técnica demostró presentar un elevado VPN (cercano al 98 %), pero un bajo valor predictivo positivo (VPP), aunque no inferior a la BEM de rutina. De igual manera que el dd-cfDNA, en los pacientes seguidos con PEG, se utilizó un menor número de BEM. (28)
El punto de corte para considerar elevado el puntaje de PEG es variable, dependiendo del riesgo inmunológico basal (pacientes sensibilizados) y del tiempo de trasplante. El mismo debe determinarse en forma seriada, dado que puede variar con el tiempo. (29,30,31) Respecto de las limitaciones del PEG, no permite establecer si el daño está ocurriendo al momento de la valoración y no es útil para el diagnóstico de rechazo mediado por anticuerpos, pues identifica variantes genéticas en los linfocitos, que son los responsables
del rechazo celular.
Combinación de pruebas diagnósticas
En la evidencia analizada hasta el momento acerca de las pruebas moleculares y genéticas, se consideró la utilización individual de cada técnica, pero también pueden usarse ambas simultáneamente.
La ISHLT publicó un estudio prospectivo, observacional y multicéntrico, que incluyó 2077 pacientes entre 2018 y 2021, a quienes se les practicaron las dos pruebas (PEG y dd-cfDNA). Es importante tener en cuenta que el tipo de rechazo al cual hace mención este estudio es únicamente al celular.
Los resultados se clasificaron de la siguiente manera:
-
doble negativo
-
PEG positivo / dd-cfDNA negativo
-
PEG negativo / dd-cfDNA positivo
-
doble positivo
La incidencia de rechazo celular fue muy baja para el grupo doble negativo (1,5%), y para los doble positivos 22%, con valores intermedios para los otros grupos. Utilizando esta estrategia el número de BEM disminuyó significativamente (8,8 % para el grupo doble negativo) con respecto a los niveles previos y la supervivencia a 2 años fue del 94,9 %; solo un 2,7 % presentó disfunción del injerto.
La interpretación de los resultados propuesta por los autores se expone en la Figura 2. Si ambas pruebas son negativas se interpreta que es poco probable el rechazo y si ambas son positivas es muy probable. Cuando es positivo el PEG y el dd-cfDNA negativo hay que considerar otras causas de activación inmune como infecciones, y cuando solo el dd-cfDNA es positivo es necesario descartar el rechazo celular o por anticuerpos. (32,33)
Aplicabilidad clínica y áreas de incertidumbre
¿Es la BEM el estándar de oro para diagnosticar el rechazo agudo del trasplante cardíaco?
De acuerdo con lo observado en el análisis bibliográfico, se podría decir que la BEM es el estudio complementario con mayor sensibilidad y especificidad en los primeros meses del trasplante. Más allá de las desventajas por su invasividad y posibles complicaciones, se puede decir que después del tercer mes, e incluso con mayor precisión pasados los 6 meses del trasplante, la BEM pierde sensibilidad, quedando entonces sus complicaciones como protagonistas no deseados.
Otro aspecto a destacar es que la evaluación del miocardio es parcial, dado que solo vemos pequeños fragmentos del mismo y, si bien la inflamación producida por el rechazo es sistémica, se inicia en parches. Por ende, respondiendo al primer interrogante, se puede aceptar que durante los primeros 3 meses posteriores al trasplante, la BEM continúa siendo el estándar de oro. Pasado este período, hoy en día contamos con las técnicas de PEG y el dosaje de dd-cfDNA que demostraron tener un excelente VPN para descartar la presencia de este evento, disminuyendo así la necesidad de utilizar pruebas diagnósticas invasivas.
Respecto de la capacidad de detectar rechazo, se puede decir que el dosaje de dd-cfDNA evidencia, en algunos registros, mejor sensibilidad y especificidad que el PEG, y además cuenta con la capacidad de diagnosticar tanto el rechazo celular como el mediado por anticuerpos.
El PEG nos indica si hay activación del sistema inmunológico, pero no proporciona información sobre la existencia de lesión tisular. Por lo tanto, sería un buen complemento del dosaje de dd-cfDNA. Ambas técnicas han demostrado disminuir la cantidad de biopsias por personas-año a lo largo del seguimiento.
Es importante aclarar que en la mayoría de los estudios se incluyeron pacientes de bajo riesgo inmunológico; no eran trasplantes recientes ni estaban sensibilizados y, por lo tanto, la incidencia de rechazo en estos estudios fue muy baja, por lo que no conocemos la sensibilidad y especificidad en una población general de trasplantados.
No hay estudios que evalúen su comportamiento más allá de los 5 años postrasplante. De todos modos, esto no constituye un problema clínico. Desde los 6 meses hasta los 5 años, los estudios analizados evidencian buenos resultados, y se puede detectar rechazo incluso antes que con la BEM.
El estudio IMAGE evaluó, a través de un cuestionario, cómo impactaron las distintas pruebas diagnósticas en la calidad de vida de los pacientes, con resultados francamente favorables para las menos invasivas.
Teniendo en cuenta lo analizado, se puede proponer un esquema de vigilancia combinando los distintos métodos diagnósticos, ajustando cada uno a su mejor perfil diagnóstico en las distintas etapas del seguimiento.
Así, desde el postoperatorio inmediato, hasta los 2-3 meses, el mejor método demostrado para la detección de rechazo es la BEM, dado que todos los nuevos ensayos fueron realizados en pacientes con al menos 55 días de postoperatorio.
Luego de este período, un esquema utilizando las nuevas técnicas de vigilancia permitiría detectar con mayor precocidad la presencia de rechazo y disminuir el número de BEM.
Este esquema ha sido validado únicamente en pacientes de bajo riesgo inmunológico y asintomáticos. En caso de presentar sintomatología o evidencia imagenológica, compatible con rechazo, debería efectuarse una BEM.
Teóricamente el PEG y la determinación del dd- cfDNA podrían permitir la titulación de inmunosupresores. Aún falta evidencia en este aspecto, pero algunos estudios en curso, como el MOSAIC, se plantean este objetivo. (34)
Tanto el dd-cfDNA como el PEG se están utilizando en muchos centros de trasplante, pero no aún en nuestro país, donde existe limitación de orden económico. En la mayoría de estos estudios estas técnicas se compararon con la BEM como estándar de oro. Un tema pendiente es realizar estudios de mayores dimen- siones con puntos finales clínicos como mortalidad o retrasplante.
Sin lugar a duda se trata de técnicas que brindan información valiosa, pero quedan varios aspectos por aclarar:
-
Punto de corte del dd-cfDNA
-
Punto de corte del PEG
-
Valor en una etapa más precoz del trasplante
-
Valor en población sensibilizada
-
El dd-cfDNA positivo ¿debe tratarse como un rechazo?
-
¿Es posible ajustar la dosis de los inmunosupresores según los valores de estas técnicas?
-
Generalizar la accesibilidad a las pruebas
-
Tener resultados de estudios con puntos finales clínicos
Con la información disponible en rechazo de trasplante cardíaco podemos decir, parafraseando a Antoine de Saint-Exupéry, que “lo esencial puede ser invisible al microscopio”.
Declaración de conflicto de interés
Los autores declaran no tener conflicto de intereses. (Véase formularios de conflictos de interés de los autores en la Web).
