INTRODUCCIÓN
La enfermedad cardiovascular (ECV) constituye la principal causa de morbilidad y mortalidad a nivel mundial. (1) Se encuentra en primer lugar entre las causas de discapacidad en las personas de más de 50 años de acuerdo con el Global Burden of Disease Study (2019), (2) destacando que la hipercolesterolemia continúa siendo uno de los principales determinantes del riesgo atribuible para la ECV y cerebrovascular. (3)
En Argentina, en el registro INTERASPIRE, se observó durante el seguimiento que el 55% de la población que presentó un primer evento coronario no estaba en los valores objetivo de colesterol unido a lipoproteínas de baja densidad (c-LDL) establecidos por las Guías de práctica clínica. (4) Sabemos que el evento clave que desencadena la aterogénesis es la retención de c- LDL y otras lipoproteínas ricas en colesterol, que lo movilizan dentro de la pared arterial y desempeñan así un papel crítico en la formación de la placa aterosclerótica y el desarrollo posterior de ECV. El aumento en la concentración de c-LDL se relaciona causalmente con la enfermedad cardiovascular aterosclerótica, y reducir todo lo posible el número de partículas de c-LDL y otras lipoproteínas que contienen apolipoproteína B (apoB) disminuye los eventos adversos cardiovasculares mayores (MACE, por su sigla en inglés). (5,6)
La problemática actual radica en que a pesar del control óptimo de los niveles de c-LDL a través de cambios en el estilo de vida y el tratamiento hipolipemiante, los pacientes que sobreviven a un primer evento CV presentan alto riesgo de recurrencia (7) y esto puede atribuirse a un riesgo residual no abordado, debido a la elevación de otras partículas aterogénicas: colesterol no HDL (c-no-HDL), colesterol remanente (CR) y lipoproteína (a) (Lp [a]). (8,9)
El c-no-HDL comprende todas las lipoproteínas plasmáticas excepto c-HDL: c-LDL, TRL (lipoproteínas ricas en triglicéridos, TG), que incluyen lipoproteínas de densidad intermedia (IDL), lipoproteínas de muy baja densidad (VLDL), quilomicrones, TRL remanente y Lp (a). Este parámetro denota el colesterol sérico de todas las lipoproteínas portadoras de apoB. (10). Se observó que el c-no-HDL es superior para estimar el riesgo de enfermedad cardiovascular aterosclerótica comparado con el c-LDL y eso puede deberse a que representa todas las partículas aterogénicas del colesterol. (10) Así mismo es mejor predictor de riesgo en pacientes con desórdenes metabólicos como hipertrigliceridemia, diabetes mellitus (DM) y obesidad. (11)
El valor deseable de c-no-HDL en prevención secundaria es menor de 85 mg/dL en pacientes de muy alto riesgo CV asociado a DM, síndrome coronario agudo (SCA), hipercolesterolemia familiar (HF), eventos recurrentes y enfermedad panvascular, y menor de 100 mg/dL sin estas características citadas (alto riesgo CV). (12,13) El CR comprende el contenido de colesterol de las TRL, que se puede estimar como la suma del colesterol total (CT) menos el cHDL y c-LDL. Al igual que el c-no-HDL, el CR es un factor causal de ECV y se ha puesto de manifiesto su potencial para predecir ECV independientemente del c-LDL. (12) La evidencia de ensayos clínicos aleatorizados respalda que niveles elevados de estas partículas se asocian a mayor riesgo de IAM y mortalidad por todas las causas. (14,15)
Se conoce además que el riesgo residual de estos pacientes es multifactorial y no sólo está relacionado con los factores lipídicos sino también con la persistencia de otros factores de riesgo como el aumento del índice de masa corporal (IMC), hipertensión arterial (HTA) y la diabetes mellitus (DM). (8,9) El objetivo principal de este estudio es determinar el rol del c-no-HDL y del CR como predictores de reincidencia de eventos cardiovasculares ateroscleróticos en pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST).
MATERIAL Y MÉTODOS
Diseño y población de estudio
Se realizó un estudio de cohorte retrospectivo en un solo centro de alta complejidad de la Ciudad Autónoma de Buenos Aires. Se incluyeron pacientes mayores de 18 años de edad que cursaron hospitalización por infarto agudo de miocardio con elevación del segmento ST (IAMCEST), con IAM de mecanismo tipo 1 evidenciado por angiografía invasiva. Se definió como pacientes con IAMCEST a aquellos pacientes que cumplían con los criterios de la cuarta definición de IAM (16) y presentaban cambios electrocardiográficos compatibles con elevación del segmento ST en el punto J en al menos dos derivaciones contiguas, mayor de 0,25 mV en hombres menores a 40 años, mayor de 0,20 mV en hombres de al menos 40 años, o mayor de 0,15 mV en mujeres en derivaciones V2-V3 y/o mayor o igual a 0,10 mV en todas las derivaciones.
Los niveles séricos de CT, c-HDL y TG se midieron en muestras de sangre venosa obtenidas dentro de las primeras 12 horas desde la admisión hospitalaria. En los casos en que fue posible, las muestras se obtuvieron en estado de ayuno (mínimo 8 horas), aunque dicha condición no fue registrada. El c-LDL fue estimado mediante la fórmula de Friedewald: c-LDL = CT - c-HDL - (TG / 5), expresado en mg/dL. El cno-HDL se calculó como la diferencia entre el CT y el c-HDL, mientras que el CR se calculó mediante la fórmula CT - c-HDL - c-LDL. Como objetivo terapéutico, y dado que se trataba de pacientes con muy alto riesgo cardiovascular, se definió un valor deseado de c-LDL < 55 mg/dL o una reducción de al menos el 50 % respecto al valor basal.
El desenlace de interés fue el combinado de angina inestable y evento adverso cardiovascular mayor (MACE), que se definió como muerte de origen cardiovascular, accidente cerebrovascular (ACV) e IAM no fatal durante los primeros 12 meses de seguimiento desde el evento índice. El seguimiento se realizó principalmente a través de la historia clínica electrónica. Aquellos pacientes que no presentaban seguimiento en nuestra institución fueron contactados telefónicamente.
Análisis estadístico
El análisis estadístico se realizó con el software R Studio, versión 1.4.1106 (The R Foundation for Statistical Computing, Viena, Austria). Las variables continuas se expresan como media y desviación estándar o mediana y rango intercuartílico (RIC), según su tipo de distribución. Las variables cualitativas se expresan como frecuencias absolutas y porcentajes. Las variables cualitativas se compararon mediante la prueba de chi cuadrado o la prueba exacta de Fisher, mientras que las variables continuas con distribución paramétrica y no paramétrica se compararon mediante la prueba de t de Student y la prueba de la U de Mann Whitney, respectivamente. Se utilizó regresión de Cox para la búsqueda de predictores independientes de eventos cardiovasculares en el seguimiento. Todos los modelos fueron ajustados por edad, género, HTA, DM, tabaquismo, CR, c-LDL y c-no- HDL. Además, se elaboraron curvas de sobrevida a través del método de Kaplan y Meier.
Se consideró un valor de p < 0,05 como estadísticamente significativo.
RESULTADOS
Características de los pacientes
Se incluyeron 403 pacientes con IAMCEST; el 78,8% era de género masculino y la mediana de edad fue de 64 años (RIC 55-73). Se analizaron los principales factores de riesgo cardiovascular, observándose una prevalencia de DM, HTA, dislipidemia y tabaquismo activo del 16%, 43%, 29% y 12%, respectivamente. En cuanto al perfil lipídico, los pacientes presentaron medianas de c-LDL, c-HDL, TG y c-no-HDL de 64 mg/dL, 36 mg/ dL, 114 mg/dL y 87 mg/dL, respectivamente. Durante el seguimiento medio de 12 ± 3 meses se verificó una adherencia al tratamiento con estatinas del 97,8%.
Eventos en el seguimiento según el cambio en el colesterol no HDL
Noventa y cinco pacientes (23,5%) desarrollaron el desenlace cardiovascular durante el seguimiento.
Los pacientes que presentaron MACE tenían valores más elevados de CT, TG, c-no-HDL,y CR. No hubo diferencias en los niveles de c-LDL.
La descripción de la población y su relación con el desarrollo de eventos se puede observar en la Tabla 1. En un análisis estratificado los pacientes que presentaron eventos en el seguimiento tenían c-no-HDL y CR más elevado que los que no, a pesar de tener valores de c-LDL en meta (Figura 1).
Tabla 1
Características basales de la población y relación con eventos adversos cardiovasculares mayores (MACE)
| MACE | ||||
|---|---|---|---|---|
| Variables | Total | No | Sí | p |
| Pacientes | 403 (100) | 308 (76,5) | 95 (23,5) | |
| Género masculino | 316 (78,8) | 250 (81,7) | 66 (69,5) | 0,016 |
| Edad, años | 64 (55-73) | 63 (54, 71) | 67,50 (57, 77) | 0,009 |
| DM | 67 (16,6) | 54 (17,5) | 13 (13,7) | 0,470 |
| TBQ | 50 (12,4) | 46 (14,9) | 4 (4,2) | 0,009 |
| DLP | 118 (29,3) | 84 (27,3) | 34 (35,8) | 0,143 |
| HTA | 175 (43,4) | 127 (41,2) | 48 (50,5) | 0,139 |
| Adherencia a estatinas | 394 (97,8) | 303 (98,4) | 91 (95,8) | 0,274 |
| c-LDL | 64 (50-85) | 64 (50-80) | 65 (52-94) | 0,327 |
| c-HDL | 36 (30-44) | 35 (30-42) | 39 (30-48) | 0,151 |
| TG | 114 (84-69) | 109,50 (79-160) | 140 (100-196) | <0,001 |
| CT | 124 (103-49) | 121 (102-140) | 138 (118-177) | <0,001 |
| c-no-HDL | 87 (70-110) | 84 (69-105) | 102 (75-135) | <0,001 |
| CR | 22 (13-33) | 20 (14-31) | 29 (17-48) | <0,001 |
| Seguimiento en meses | 4 (1-10) | 6 (1-11) | 1 (1-4) | <0,001 |
Las variables cualitativas se presentan como frecuencia y porcentaje. Las variables cuantitativas como mediana y rango intercuartílico c-HDL: colesterol asociado a lipoproteínas de alta densidad; c-LDL: colesterol asociado a lipoproteínas de baja densidad; c-no-HDL: colesterol no asociado a lipoproteínas de alta densidad; CR: colesterol remanente; CT: colesterol total; DLP: dislipidemia; DM: diabetes mellitus; HTA: hipertensión arterial; TBQ: tabaquismo; TG: triglicéridos
Fig. 1.
La Figura 1A muestra la relación entre el CR y el c-no- HDL según niveles de c-LDL. En ambos grupos se observa una asociación lineal positiva entre ambas variables. Sin embargo, la pendiente correspondiente al grupo con c-LDL < 55 mg/dL (línea azul) se sitúa por encima, lo que indica que, para un mismo valor de CR, estos pacientes presentaron niveles más elevados de c- no-HDL. La Figura 1B muestra la comparación de los niveles de c- no-HDL según la presencia de eventos (MACE), estratificados por niveles de c-LDL. En ambos estratos, los pacientes que presentaron eventos (rojo) mostraron niveles significativamente más altos de c-no-HDL en comparación con aquellos sin eventos (azul), con diferencias estadísticamente significativas.
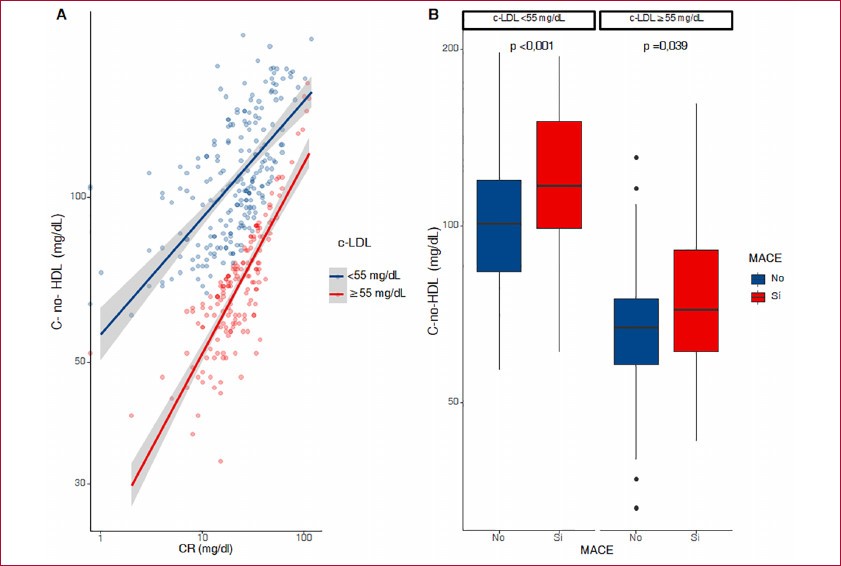
c-LDL: colesterol asociado a lipoproteínas de baja densidad; c-no-HDL: colesterol no asociado a lipoproteínas de alta densidad; CR: colesterol remanente; MACE: eventos adversos cardiovasculares mayores
Análisis multivariado: Predictores independientes de eventos cardiovasculares mayores
Se ajustaron dos modelos predictivos por regresión de Cox, uno con la variable c-LDL y otro con la variable c-no-HDL. El c-LDL presentó un HR (IC 95%) de 1,15 (0,94-1,39, p=0,166) mientras que el c-no-HDL presentó un HR de 1,45 (1,21-1,73, p < 0,001). (Figura 2).
Fig. 2
Modelo de Cox para eventos adversos cardiovasculares mayores (MACE)
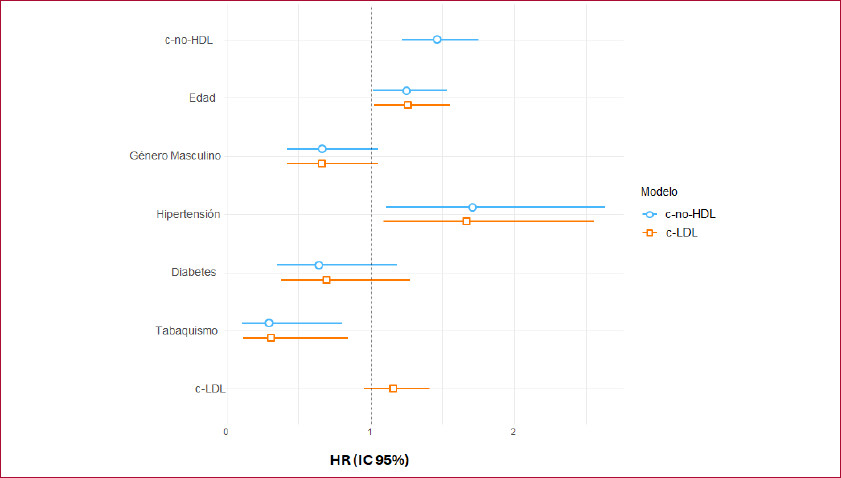
c-LDL: colesterol asociado a lipoproteínas de baja densidad; c-no-HDL: colesterol no asociado a lipoproteínas de alta densidad; HR: hazard ratio; IC 95%: intervalo de confianza del 95%
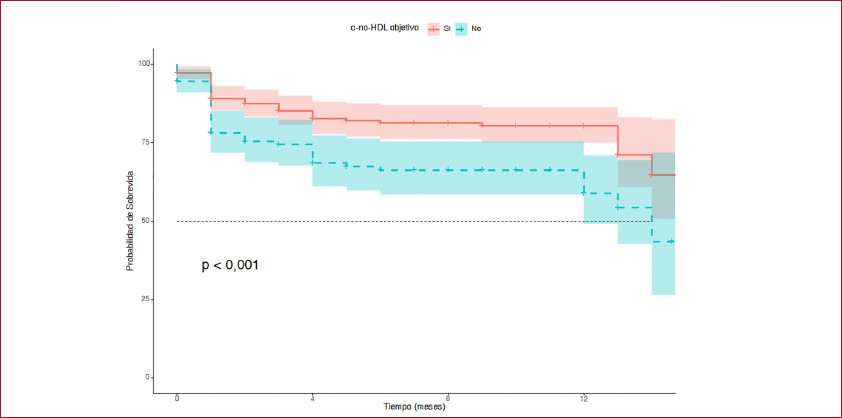
Los pacientes con valores de c-no-HDL en meta presentaron mayor sobrevida libre de eventos en el seguimiento (p=0,001) (Figura 3).
DISCUSIÓN
El 23,5% de los pacientes incluidos presentaron MACE durante el primer año de seguimiento tras el evento inicial. No se observaron diferencias significativas en relación a la ocurrencia de eventos de acuerdo con los niveles de c-LDL. En cambio, los pacientes con MACE mostraron valores fuera de meta de c-no-HDL y CR, con medianas de 102 mg/dL y 29 mg/dL, respectivamente. Además, el c-no-HDL se identificó como un predictor independiente de eventos cardiovasculares mayores durante el seguimiento, a diferencia del c-LDL, que no mostró tal asociación.
En el registro SWEDEHEART, (17) que incluyó a 56 262 pacientes con IAM como primer evento cardiovascular, se observó que el 17% de ellos presentó MACE en el seguimiento. Por otro lado, en dos ensayos clínicos (ODYSSEY y FOURIER), diseñados para evaluar la eficacia de los inhibidores de proproteína convertasa subtilisina/kexina tipo 9 (PCSK9), alirocumab y evolocumab respectivamente en comparación con placebo para la reducción del c-LDL y la disminución de MACE, se observó que, a pesar de alcanzar niveles críticos de reducción de c-LDL (medianas de 38 mg/dL y 30 mg/ dL respectivamente) los pacientes que recibieron anticuerpos monoclonales desarrollaron MACE durante el seguimiento en un 9,5% y 12,6%, respectivamente. (18,19) En nuestra cohorte, los pacientes con un nuevo evento durante el seguimiento mostraron una mediana de c-LDL de 64 mg/dL, un valor muy cercano a los objetivos sugeridos por las guías internacionales.
En el metanálisis de Boekholdt y cols. (20) se c-no-HDL. Incluso, aquellos pacientes con c-LDL en observó una fuerte asociación entre los valores de meta, pero no para el c-no-HDL presentaron un HR c-LDL y c-no-HDL como predictores de MACE en de 1,32 (IC 95% 1,17-1,50; p < 0,001). Así mismo, en el seguimiento, pero la asociación fue mayor para el el registro sueco mencionado previamente, (17) se realizaron mediciones basales del c-no-HDL al ingreso y al año de seguimiento y se observó una incidencia acumulada por cuartil de reducción del c-no-HDL con clara separación de las curvas de sobrevida, evidenciando que una mayor reducción del c-no-HDL (≥ 85 mg/dL) se asoció con una menor tasa de eventos adversos en el seguimiento. Los pacientes en el cuartil con la mayor reducción presentaron un 37% menos de riesgo de MACE (HR 0,63; IC 95% 0,57-0,68), un 21% menos de riesgo de mortalidad por cualquier causa y un 49% menos de riesgo de IAM no fatal (p < 0,001). Además, el riesgo de MACE al año de seguimiento fue significativamente menor en los pacientes que alcanzaron tempranamente el objetivo de c-no-HDL y lo mantuvieron durante el primer año de seguimiento (HR 0,80; IC 95% 0,74-0,86). Estos resultados destacan la importancia de iniciar el tratamiento y alcanzar las metas de c-no-HDL en forma precoz luego del evento índice, lo que optimiza los beneficios clínicos a largo plazo. Estos hallazgos son similares a los encontrados en nuestro estudio, en que el c-no-HDL se comportó como un predictor independiente de eventos con HR de 1,45 (IC 95% 1,21-1,73, p <0,001).
Por otro lado, en dos ensayos clínicos aleatorizados que analizaron las discordancias entre los niveles de apoB, c-no-HDL y c-LDL para evaluar el riesgo residual de IAM, se evidenció que los niveles elevados de apoB y c-no-HDL, pero no de c-LDL, se asociaron con un mayor riesgo de IAM y mortalidad por todas las causas. Por el contrario, un c-LDL elevado, discordante con niveles bajos de apoB o c-no-HDL, no mostró tal asociación. (7, 21,22,23) Si bien nuestro estudio no incluyó la determinación de apoB, estos hallazgos subrayan la importancia de considerar otros parámetros lipídicos, además del c-LDL, para una mejor evaluación del riesgo residual en nuestros pacientes.
A pesar de que en nuestro estudio el c-LDL no se comportó como un predictor significativo de eventos, su rol clínico continúa plenamente vigente. El c-LDL sigue siendo uno de los principales objetivos terapéuticos en prevención cardiovascular, y su reducción intensiva ha demostrado beneficios en múltiples estudios y registros. Las principales guías internacionales, como las del American College of Cardiology (ACC) y la Sociedad Europea de Cardiología (ESC/EAS), recomiendan alcanzar niveles de c-LDL < 55 mg/dL en pacientes de muy alto riesgo cardiovascular (6,24). Por lo tanto, nuestros hallazgos no deben interpretarse como una desestimación de la utilidad clínica del c-LDL, sino como un llamado a ampliar el enfoque hacia otros parámetros lipídicos complementarios en la evaluación del riesgo residual.
Limitaciones
Nuestro estudio presenta varias limitaciones que merecen consideración. En primer lugar, debido a la naturaleza retrospectiva del estudio, no se dispuso de información completa en cuanto al tratamiento hipolipemiante, sobre ajuste de medicación durante el seguimiento y la adherencia de los pacientes. Estos datos estuvieron supeditados al registro en la historia clínica electrónica y comunicación telefónica en algunos casos. En segundo lugar, el registro y seguimiento de los pacientes se limitaron a un solo centro, por lo que nuestros resultados representan la realidad del centro participante. Otra limitación metodológica relevante es que el c-LDL fue estimado mediante la fórmula de Friedewald, que puede perder precisión diagnóstica en presencia de trigliceridemia moderada o elevada. Esta situación, frecuente en pacientes de alto riesgo cardiovascular, podría haber llevado a una subestimación del valor real de c-LDL, particularmente en aquellos con niveles de TG ≥200 mg/dL. Por último, no incluimos el perfil lipídico basal, lo cual impidió calcular la reducción absoluta y porcentual de las distintas fracciones lipídicas durante el seguimiento.
CONCLUSIÓN
Nuestro estudio destaca que, incluso con niveles de c-LDL cercanos a los objetivos recomendados por las guías, un porcentaje significativo de pacientes sigue enfrentando un alto riesgo de eventos cardiovasculares mayores. El c-no-HDL demostró ser un marcador clave para identificar este riesgo residual, subrayando la necesidad de considerarlo como una herramienta complementaria para optimizar las estrategias de prevención y manejo en estos pacientes.
Declaración de conflicto de Intereses
Los autores declaran que no tienen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la Web).