INTRODUCCIÓN
La miocardiopatía hipertrófica (MCH) es una enfermedad genética frecuente y heterogénea, con una prevalencia estimada de 1 en 200 a 1 en 500 personas. Puede presentarse con síntomas variables y complicaciones graves como insuficiencia cardíaca, arritmias y muerte súbita. (1) Se clasifica en obstructiva (MCHO), caracterizada por obstrucción dinámica del tracto de salida del ventrículo izquierdo (TSVI), y no obstructiva (MCHNO). Aunque existen tratamientos convencionales, algunos pacientes presentan síntomas refractarios o requieren intervenciones invasivas. En este contexto, los inhibidores de miosina han surgido como una nueva estrategia terapéutica para abordar los mecanismos fisiopatológicos subyacentes de la enfermedad. (2,3). En este artículo se revisarán su mecanismo de acción, la evidencia disponible, las indicaciones y formas de uso, así como los efectos adversos asociados.
MECANISMOS DE ACCIÓN
La hipercontractilidad miocárdica es una de las características centrales de la MCH. Este fenómeno resulta de alteraciones en la interacción actina-miosina, frecuentemente originadas por mutaciones en genes sarcoméricos. Además de contribuir a la obstrucción dinámica del TSVI, la hipercontractilidad favorece el desarrollo de desarreglos miofibrilares y fibrosis miocárdica. (4,5)
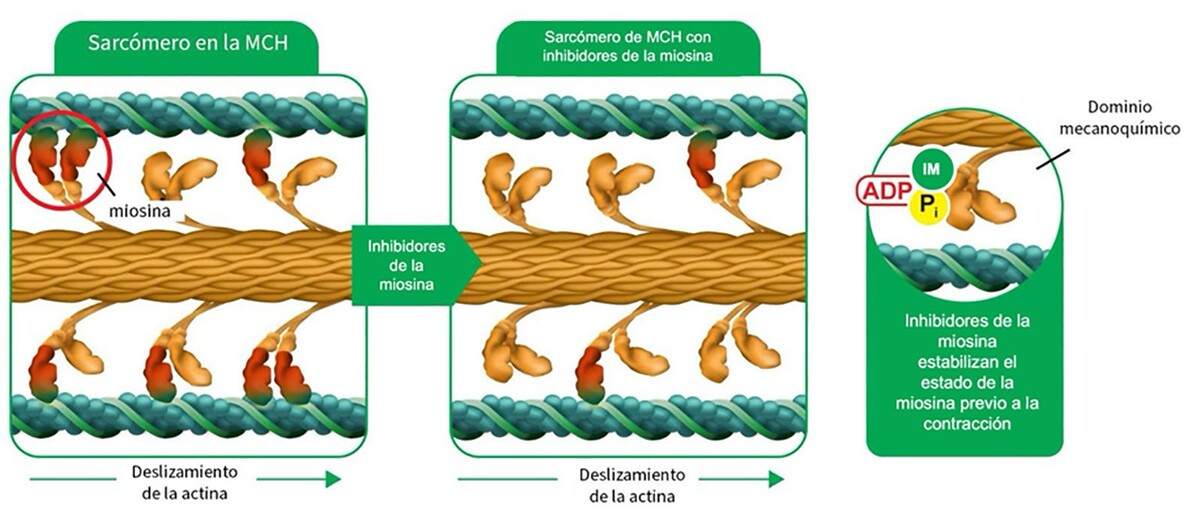
Los antagonistas de la miosina, como el mavacamten y el aficamten, actúan modulando directamente la interacción actina-miosina, con reducción de la fuerza de contracción y atenuación del estado hipercontráctil crónico de los miocitos. Estos fármacos inhiben selectivamente la ATPasa de miosina cardíaca, disminuyendo la formación de puentes cruzados entre actina y miosina, lo que resulta en menor contractilidad miocárdica. Además, estabilizan el estado de súper relajación de la miosina, reducen la liberación de fosfato inorgánico y limitan la interacción de la miosina con la actina, lo que contrarresta la hipercontractilidad observada en la MCH. (6) (Figura 1)
ADP: difosfato de adenosina; IM: inhibidores de la miosina; MCH: miocardiopatía hipertrófica; Pi: fosfato inorgánico
Estos agentes aumentan la proporción de moléculas de miosina en estado de súper relajación y favorecen la cinética del desprendimiento de los puentes cruzados, estimulan la liberación de difosfato de adenosina (ADP) de la miosina y promueven la unión a esta del trifosfato de adenosina (ATP). Como consecuencia, no solo disminuyen la fuerza contráctil sino que también mejoran la relajación del músculo cardíaco, abordando de manera simultánea la hipercontractilidad y la disfunción diastólica, dos de los principales mecanismos fisiopatológicos de la MCH. (7-9)
FARMACOLOGÍA
El mavacamten es un inhibidor selectivo y reversible de la ATPasa de miosina cardíaca, desarrollado para modular la contractilidad miocárdica. Se administra por vía oral, en dosis de 2,5 a 15 mg, con biodisponibilidad adecuada y una vida media de aproximadamente 9 días, lo que permite su dosificación una vez al día. Su metabolismo es predominantemente hepático, mediado por el CYP2C19 y, en menor medida, por el CYP3A4 y el CYP2C9. Esto lo hace susceptible a interacciones con inhibidores e inductores de estas enzimas, lo que puede afectar su concentración plasmática y eficacia. (10)
El aficamten es un inhibidor de segunda generación de la ATPasa de miosina cardíaca. Su dosis es de 5 a 20 mg, su vida media más corta que la del mavacamten (28 a 40 horas), lo que permite ajustes más rápidos en la dosificación y menor riesgo de acumulación. También se administra por vía oral y su metabolismo es hepático, mediado principalmente por el CYP3A4, con menor contribución de otras enzimas del citocromo P450. En comparación con el mavacamten, tiene menos interacciones farmacológicas relevantes y un perfil de seguridad más predecible, sin necesidad de ajuste de dosis en función del CYP2C19. (10,11)
Los estudios disponibles sugieren que ambas drogas no se excretan en forma significativa por vía renal. Sin embargo, la farmacocinética en pacientes con insuficiencia renal grave no está completamente caracterizada. En presencia de insuficiencia hepática moderada a grave podría haber acumulación del fármaco, aunque los datos clínicos en estos pacientes son limitados.
El mavacamten y el aficamten están contraindicados durante el embarazo debido a su mecanismo de acción, que puede afectar el desarrollo cardiovascular fetal, por lo que se recomienda el uso de métodos anticonceptivos eficaces en mujeres en edad fértil durante el tratamiento y hasta al menos cuatro meses después de la suspensión.
EVIDENCIA EN PACIENTES CON MCHO
Ensayos clínicos
El desarrollo clínico del mavacamten comenzó con el estudio fase 2 PIONEER-HCM, que incluyó pacientes con MCHO sintomática y demostró reducción significativa del gradiente obstructivo del TSVI, tanto en reposo como postejercicio. Los pacientes tratados con mavacamten experimentaron mejora en la clase funcional de la NYHA y una reducción del fragmento aminoterminal del propéptido natriurético tipo B (NTproBNP). Además, el consumo pico de oxígeno (VO2 pico) aumentó en un promedio de 1,5 mL/kg/min, lo que reflejó una mejora en la capacidad funcional. (12).
Estos resultados llevaron al ensayo fase 3 EXPLORER-HCM, donde se confirmó la eficacia del mavacamten en la reducción del gradiente del TSVI, con una disminución promedio de 40 mmHg. Además, el 65 % de los pacientes tratados presentaron una mejoría en al menos un punto de la escala funcional de la NYHA, y el VO2 pico aumentó 1,4 mL/kg/min en comparación con el placebo. (13). En términos ecocardiográficos, un 80,9% de los pacientes en la rama de mavacamten lograron la resolución completa del movimiento anterior sistólico de la válvula mitral a las 30 semanas, lo que sugiere un impacto significativo en la fisiopatología de la enfermedad. (14)
El estudio fase 3 VALOR-HCM evaluó el mavacamten en pacientes con MCHO grave, con indicación de terapia de reducción septal. Tras 16 semanas de tratamiento, el 82 % de los pacientes en la rama de mavacamten ya no cumplía criterios para intervención, en comparación con solo el 23 % en el grupo placebo. Se observó una reducción del gradiente del TSVI de 51 mmHg a 14 mmHg, con mejoría en la clase funcional de la NYHA y un aumento en el VO2 pico de 1,7 mL/ kg/min. (15)
Los datos a largo plazo provienen del estudio MAVALTE, que incluyó pacientes previamente tratados en EXPLORER-HCM, con un seguimiento de 80 semanas. Los resultados confirmaron una reducción progresiva y sostenida en los gradientes del TSVI, pasando de 48 mmHg a 10 mmHg, así como una disminución significativa del NT-proBNP de 783 ng/L a 123 ng/L. Además, el 60,2 % de los pacientes mantuvo mejoría de su clase funcional. Estos hallazgos sugieren que el mavacamten no solo tiene un efecto sintomático a corto plazo, sino que podría modificar la progresión de la enfermedad. (16)
Por su parte, el aficamten ha mostrado un perfil de eficacia similar. En el ensayo fase 2 REDWOOD-HCM, el tratamiento con aficamten resultó en una reducción significativa del gradiente obstructivo de 36 mmHg, acompañada de una mejoría en la clase funcional de la NYHA y una disminución del NT-proBNP. (17). En el estudio fase 3 SEQUOIA-HCM, el aficamten logró una mejoría del consumo máximo de oxígeno de 1,9 mL/kg/min, con un perfil de seguridad favorable y una baja incidencia de reducción de la fracción de eyección ventricular izquierda (FEVI). (18) Un estudio clave recientemente publicado es MAPLE-HCM, el primero en comparar un inhibidor de la miosina frente a terapia estándar. Este ensayo fase 3 aleatorizó pacientes con MCHO sintomática a recibir aficamten o metoprolol. A las 24 semanas, el aficamten logró una reducción significativa del gradiente del TSVI (-40,7 mmHg) en contraste con la modesta reducción observada con metoprolol (-3,8 mmHg; p<0,001). Asimismo, se documentaron mejoras superiores con aficamten en la capacidad funcional (VO2 pico: +1.1 vs -1,2 ml/kg/ min; p=0,001) y en la calidad de vida (score KCCQCSS: +15,8 vs +8.7 puntos p=0,002). En cambio, el tratamiento con metoprolol no se asoció con mejoría significativa en los parámetros funcionales ni sintomáticos. El perfil de seguridad del aficamten fue favorable, con descensos transitorios de la FEVI por debajo de 50 % en el 1 % de los pacientes, todos reversibles. Estos hallazgos refuerzan la hipótesis de que, a diferencia de los betabloqueantes, los inhibidores de la miosina como el aficamten actúan directamente sobre el mecanismo fisiopatológico de la obstrucción y podrían redefinir el tratamiento inicial de la MCH obstructiva. (19)
En la Tabla 1 se resumen los ensayos clínicos realizados con mavacamten y aficamten.
Tabla 1
Principales ensayos clínicos completados y publicados de inhibidores de la miosina en pacientes adultos con MCHO
| Estudio (droga) | Tipo de estudio | Punto finales | Resultados |
|---|---|---|---|
| PIONEER-HCM (mavacamten*) 2019 (12) | Fase II, multicéntrico, abierto, no randomizado, n=21 Cohorte A (n=11): dosis inicial 10 o 15 mg Cohorte B: (n=10): titulación lenta desde 2 a 5 mg | Reducción de gradientes del TSVI en ejercicio a 12 semanas. Valoración de VO2 pico | Cohorte A: cambio medio de -89,5 mmHg y de 3,5 mL/kg/ min Cohorte B: cambio medio de 25 mmHg y de 1,7 mL/kg/min |
| EXPLORER-HCM (mavacamten) 2020 (13) | Fase III, multicéntrico, randomizado, doble ciego, controlado con placebo, n=251 Grupo activo n=128 Placebo n=123 | Aumento de 1,5 mL/kg/min o más en VO2 pico + reducción de 1 punto en la CF NYHA ó aumento > 3 mL/kg/min del VO2 pico sin empeorar la CF NYHA a 30 semanas | 37% grupo mavacamten vs 17% placebo (p = 0,0005) VO2 pico: + 1,4 mL/kg/min en mavacamten vs +0,1 mL/kg/ min en el grupo placebo (p = 0,0006) Gradiente: -35,6 mm Hg, p < 0,0001 |
| VALOR-HCM (mavacamten) 2022 (15) | Fase III, multicéntrico, randomizado, doble ciego, controlado con placebo n=112. | Mejoría que implique salir de indicación de reducción septal a 16 semanas | Continuaron con indicación: 18% con mavacamten vs 77% con placebo, p<0,001 Gradiente: -37,2 mm Hg vs. placebo, p < 0,001 |
| REDWOOD (aficamten**) 2023 (17) | Fase II, multicéntrico Pacientes con gradiente de TSVI en reposo ≥30 mmHg o provocado ≥50 mmHg. Asignación 2:1 aficamten/ placebo 10 semanas | Cambios en gradiente del TSVI, FEVI y CF NYHA | -40 mmHg en el gradiente del TSVI en reposo y de -36 mmHg en Valsalva en la Cohorte 1, y de -43 mmHg en reposo y -53 mmHg durante Valsalva en la Cohorte 2. |
| SEQUOIA-HCM (aficamten) 2024 (18) | Fase III, multicéntrico, randomizado, doble ciego, controlado con placebo n=282 Grupo activo n=142 Placebo n=140 | Cambio en consumo de oxígeno pico a las 24 semanas Calidad de vida | Aumento de 1,8 mL/kg/min en grupo aficamten vs. 0,0 mL/kg/ min en placebo. ≥20 puntos en la puntuación del KCCQ-CSS: 29,7% vs. 12,4% en placebo |
| MAPLE -HCM (aficamten) 2025 (19) | Fase III, multicéntrico, randomizado, doble ciego, aficamten vs metoprolol Aficamten n=87 Metoprolol n=88 | Cambio en consumo de oxígeno a las 24 semanas Calidad de vida | VO2 pico: 1,1 mL/kg/min en aficamten y -1,2 mL en metoprolol; p=0,001 gradiente del TSVI: -40,7 mmHg vs. -3,8 mmHg; p<0,001 KCCQ-CSS: +15,8 vs +8,7 puntos p=0,002. |
* Mavacamten aprobado por Food Drug Administration (FDA), European Medicines Agency (EMA), y Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT).
** Aficamten aún no aprobado por FDA, EMA ni ANMAT.
CF NYHA: clase funcional de la New York Heart Association; FEVI: fracción de eyección del ventrículo izquierdo; KCCQ-CSS: Kansas City Cardiomyopathy Questionnaire Clinical Summary Score; MCHO: miocardiopatía hipertrófica obstructiva; TSVI: tracto de salida del ventrículo izquierdo;
Seguridad
En términos de seguridad, ambos fármacos han sido bien tolerados. Entre el 6 y 7 % de los pacientes tratados con mavacamten desarrollaron una FEVI <50 %, lo que llevó a la necesidad de suspender temporalmente el tratamiento en algunos casos. Sin embargo, esta disfunción fue reversible con la interrupción del fármaco. En el caso del aficamten, menos del 2 % de los pacientes presentaron una FEVI <50 %, y en la mayoría de los casos la función ventricular se normalizó tras la reducción de la dosis. (13,18)
Eventos duros
A pesar de los beneficios observados en términos de síntomas, consumo de oxígeno y biomarcadores, hasta la fecha no hay evidencia clara de que el mavacamten o el aficamten reduzcan la mortalidad o la incidencia de arritmia ventricular en pacientes con MCHO. No se han demostrado reducciones en la mortalidad, ya que los ensayos clínicos han sido diseñados con puntos finales funcionales y de calidad de vida, sin evaluar específicamente la sobrevida a largo plazo. Tampoco hay evidencia concluyente de que estos fármacos disminuyan la carga arrítmica o el riesgo de taquicardia y fibrilación ventricular, principales responsables de la muerte súbita en esta población. Se ha planteado la hipótesis de que la reducción del estrés parietal con estos agentes podría disminuir la carga arrítmica, pero hasta ahora ello no se ha evidenciado en los ensayos clínicos. En cuanto a la necesidad de implante de desfibriladores automáticos implantables, tampoco se han reportado cambios en los criterios actuales de indicación.
Si bien aún se requieren estudios con mayor seguimiento, los inhibidores de miosina representan actualmente una alternativa no invasiva para el tratamiento de pacientes con MCHO que requieren intervención septal, frente a la miectomía septal y la ablación alcohólica. Tanto la miectomía como la ablación septal son procedimientos invasivos asociados a un riesgo muy bajo de mortalidad periprocedimiento, (20,21) riesgo que no se ha observado con el uso de inhibidores de miosina.
Evidencia de la vida real
El mavacamten ha recibido la aprobación de los principales entes reguladores a nivel mundial. Sin embargo, para mitigar el riesgo de disfunción sistólica del ventrículo izquierdo, insuficiencia cardíaca e interacciones farmacológicas, su aprobación está supeditada a un programa de evaluación y mitigación de riesgos (REMS, por su sigla en inglés). Este programa establece estrategias de educación y monitoreo continuo, incluyendo la capacitación obligatoria de los profesionales de la salud y la realización de ecocardiogramas periódicos durante el seguimiento.
En este contexto, Desai y colaboradores publicaron, a finales de 2024, los resultados de los primeros 22 meses del programa REMS, aportando datos sobre el uso del fármaco en Estados Unidos. (22) Sobre un total de 5573 pacientes que recibieron al menos una dosis de la droga y presentaron los formularios correspondientes, 4,6 % presentó caída de la FEVI, 1,3 % se internó por insuficiencia cardiaca y solo 0,3 % desarrolló ambas complicaciones juntas. Los números fueron muy similares en aquellos pacientes que recibieron la medicación al menos durante un año. (22)
La dosis de fármaco utilizada fue 5 o 10 mg a los seis meses de seguimiento en la mayoría de los pacientes (74 %), y solo un 5 % requirió la dosis máxima de 15 mg en ese tiempo. El principal motivo de la disminución de dosis (95 % de los casos) fue la suficiencia terapéutica, por alcanzar un gradiente en el TSVI < 20 mmHg. Finalmente, con respecto a los gradientes en el TSVI, el 42 % persistió con gradientes en reposo por encima de 30 mmHg a los 3 meses de comenzar el fármaco, y solo el 29 % a los 6 meses de tratamiento. Como limitaciones, este programa está diseñado para asegurar que se cumplen las condiciones para el uso seguro del fármaco (pacientes con FEVI > 50 % y sin interacciones con otras drogas), sin evaluar el criterio clínico de la indicación, el motivo de la suspensión, la evolución de los síntomas o el requerimiento de terapias de reducción septal. Esto último fue evaluado en algunas cohortes del mundo real con menor número de pacientes, también con buenos resultados. (23-25) Respecto de las estrategias de seguridad, la agencia reguladora en Europa (EMA) obliga a la realización del análisis de polimorfismos en los citocromos responsables de su metabolismo previo al inicio del tratamiento para ajuste de la dosis inicial. En Argentina no es necesaria la evaluación de dichos polimorfismos y el monitoreo es dependiente de variables clínicas y ecocardiográficas.
EVIDENCIA EN PACIENTES CON MCHNO
El desarrollo clínico del mavacamten en la MCHNO comenzó con el estudio fase 2 MAVERICK-HCM, en el cual se incluyeron pacientes sintomáticos con FEVI ≥55% y ausencia de obstrucción significativa del TSVI. A las 16 semanas, se observó una reducción significativa en los niveles de NT-proBNP en el grupo tratado con mavacamten en comparación con placebo, sugiriendo una mejoría en la sobrecarga de presión y la función diastólica. Además, se registró una reducción en la rigidez ventricular, medida por el índice E/e’, aunque sin cambios significativos en la FEVI ni en la capacidad funcional medida por el consumo pico de oxígeno. (26)
Estos hallazgos condujeron al diseño del estudio de fase 3 ODYSSEY-HCM, que evaluó los efectos del mavacamten en una población de 580 pacientes con MCHNO sintomática. A las 48 semanas, el fármaco no alcanzó el objetivo primario de mejoría en el consumo pico de oxígeno (+1,0 mL/kg/min con mavacamten vs +1,3 mL/kg/min con placebo; p=NS). No obstante, se observaron beneficios en parámetros secundarios, incluyendo reducciones significativas en el NT-proBNP (-50% vs -10%; p<0,01) y troponina T ultrasensible (-22% respecto del placebo; p<0,05), así como una tendencia favorable en el score KCCQCSS (+7 vs +5 puntos). En cuanto a la seguridad, un hallazgo relevante fue que el 21,5 % de los pacientes tratados con mavacamten desarrolló una FEVI <50 %, en la mayoría de los casos reversible tras la interrupción del tratamiento. Estos resultados sugieren que, aunque el mavacamten reduce la carga hemodinámica y los biomarcadores de estrés miocárdico, su efecto en la capacidad funcional global es limitado. Como posible explicación, se ha planteado que la dosis utilizada pudo haber sido excesiva y el tiempo de exposición relativamente corto, lo que podría haber atenuado el beneficio clínico neto observado en esta población. (27)
En el caso del aficamten, el ensayo fase 2 FOREST-HCM ha mostrado resultados preliminares alentadores, con una reducción en NTproBNP y mejoría en parámetros ecocardiográficos de disfunción diastólica. (28) Actualmente se encuentra en curso el estudio fase 3 ACACIA-HCM, que evaluará la eficacia y seguridad del aficamten en una cohorte amplia de pacientes con MCHNO, y proporcionará evidencia clave sobre su impacto en la función cardíaca y los síntomas.
TITULACIÓN DE LA MEDICACIÓN
El mavacamten se administra en forma oral, en cápsulas de 2,5 mg, 5 mg, 10 mg y 15 mg. La forma de uso, dosis y titulación se basan en el esquema utilizado en el estudio EXPLORER-HCM. (13)
La dosis inicial recomendada es de 5 mg una vez al día. Se sugiere ajustar la dosis cada 4 semanas, con un límite máximo de una dosis diaria de 15 mg.
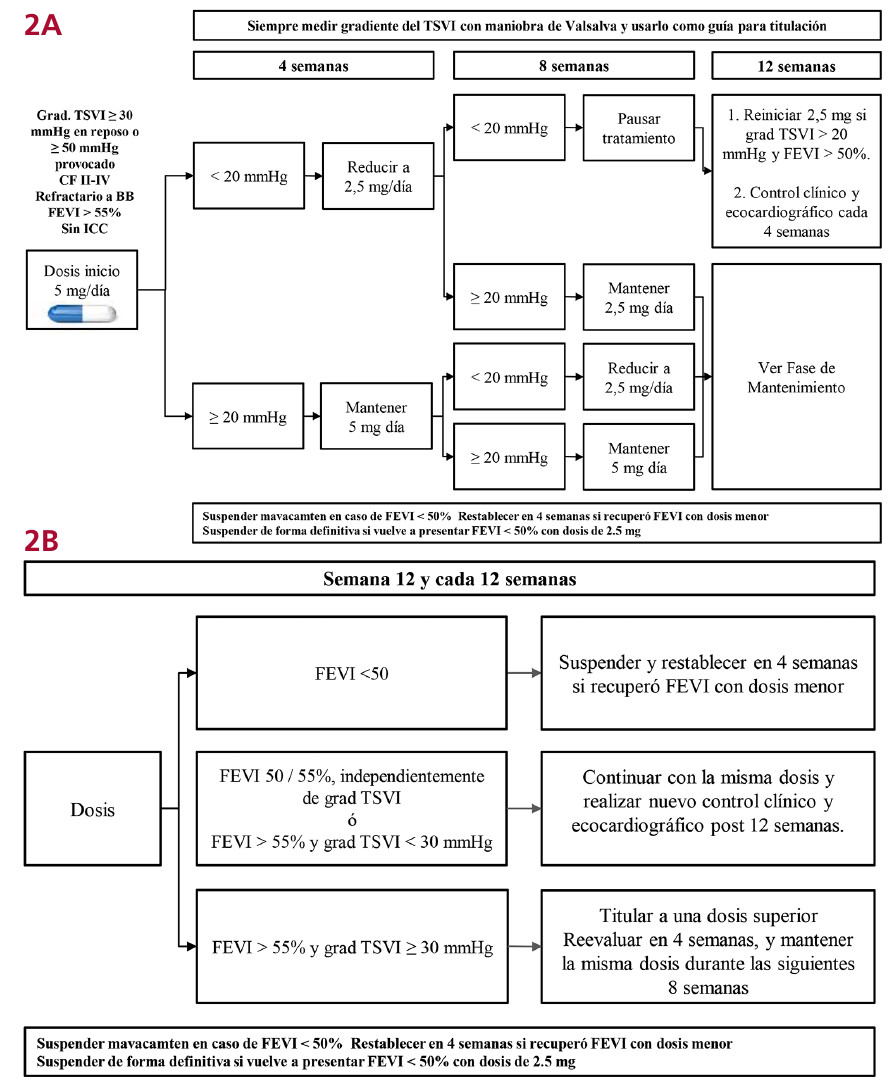
Es imprescindible un estricto monitoreo clínico para identificar posibles signos de IC, complementado con un control ecocardiográfico enfocado principalmente en la evaluación de la FEVI y el gradiente del TSVI, tanto antes del inicio del tratamiento como durante el seguimiento posterior. No se recomienda el inicio del tratamiento en pacientes con FEVI < 50 %. Una vez iniciado, se recomienda seguir el esquema de la Figura 2. (adaptado de 29)
CF: clase funcional; FEVI: fracción de eyección del ventrículo izquierdo; grad: gradiente; TSVI: tracto de salida del ventrículo izquierdo
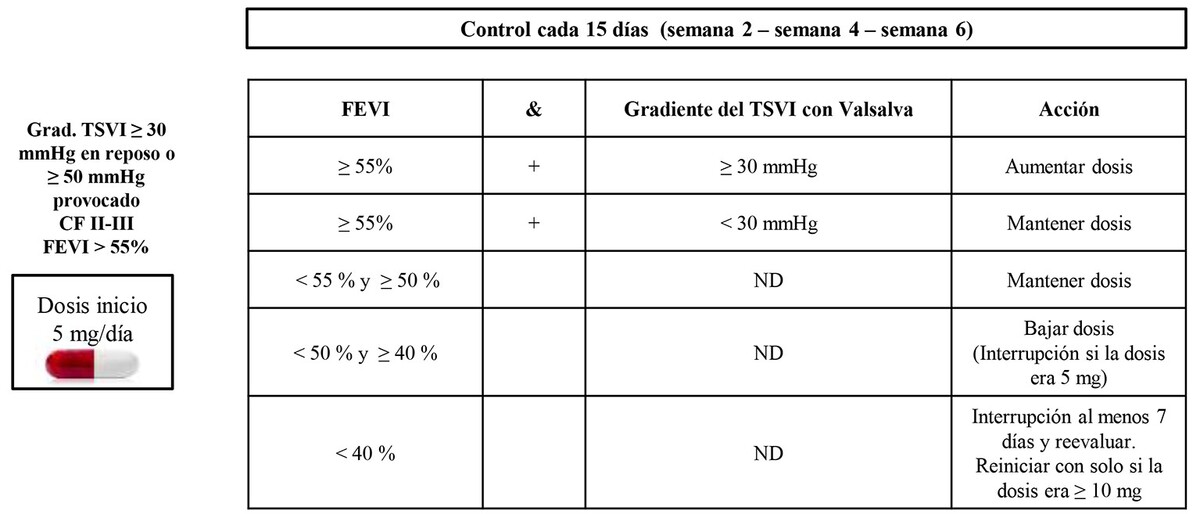
En el caso del aficamten la dosis inicial es de 5 mg una vez al día con ajustes cada 2 semanas debido a la menor vida media. En la Figura 3 se esquematiza el algoritmo de titulación utilizado en el estudio de fase III SEQUOIA-HCM. (18)
FEVI: fracción de eyección del ventrículo izquierdo; CF: clase funcional; ND: no disponible; TSVI: tracto de salida del ventrrículo izquierdo
Interacciones farmacológicas clínicamente relevantes y frecuentes
Dado el metabolismo a través del sistema de citocromos (mayoritariamente CYP2C19), debe evitarse el uso de mavacamten con medicamentos como ciertos antifúngicos, ciertos antibióticos macrólidos, algunos antidepresivos e inhibidores de proteasa, entre otros; así como también el jugo de pomelo. Antes del inicio del mavacamten deben haberse suspendido por al menos 14 días inhibidores de CYP2C19 e inhibidores fuertes de citocromos CYP3A4. En el caso del aficamten, éste no interactúa con el sistema de citocromos, por lo que no existiría dicha interacción y no serían necesarias mayores precauciones. En la Tabla 2 se resumen algunas de las interacciones farmacológicas relevantes para el mavacamten.
Tabla 2
Interacciones farmacológicas relevantes para mavacamten
| Grupo | Efecto | Ejemplo | Recomendación |
|---|---|---|---|
| Inhibidores de alta potencia del 2C19 | Aumenta concentración plasmática de Mavacamten | Fluoxetina, modafinilo, ritonavir | No combinar |
| Inhibidores alta potencia del 3A4 | Aumenta concentración plasmática de Mavacamten | Claritromicina, itraconazol, ritonavir, lopinavir, loperamida, efavirenz | No combinar |
| Inhibidores de moderada potencia 2C19 | Aumentan levemente la concentración de mavacamten | Sertralina, efavirenz, pantoprazol, lansoprazol, omeprazol, claritromicina | Bajar dosis a 2,5 mg cuando se inicia uno de estos fármacos |
| Inhibidores de moderada potencia 3A4 | Aumentan levemente la concentración de mavacamten | Eritromicina, fluconazol, amiodarona, diltiazem, verapamilo, jugo de pomelo | Bajar dosis a 2,5 mg cuando se inicia uno de estos fármacos |
| Inductores del 3A4 y 2C19 | Disminuyen concentración de mavacamten y ante su suspensión la aumentan | Rifampicina, fenitoína, dexametasona, modafinilo, efavirenz | Precaución ante la suspensión de alguno de ellos |
COSTO-EFECTIVIDAD
El costo elevado del mavacamten plantea interrogantes sobre su costo-efectividad en comparación con otras estrategias terapéuticas. Si bien ofrece beneficios clínicos significativos, su precio actual podría situarlo fuera del umbral de costo-efectividad generalmente aceptado en algunos sistemas de salud.
Un análisis realizado en Estados Unidos por el Instituto de Revisión Clínica y Económica (ICER) determinó que, para que el mavacamten sea considerado costo-efectivo según los umbrales utilizados en ese país, su precio anual debería ser inferior a 15 000 dólares (lejos de los 85 000 actuales). (30) Sin embargo, estas conclusiones no son directamente aplicables a otros sistemas de salud, ya que los costos de tratamientos y procedimientos varían considerablemente entre países.
Si bien el mavacamten podría reducir la necesidad de procedimientos invasivos y mejorar la calidad de vida de los pacientes, el costo sigue siendo un desafío para su implementación generalizada. Su viabilidad económica dependerá de estrategias de acceso, negociación de precios y estudios adicionales que permitan evaluar su impacto en la práctica clínica real.
En cuanto al aficamten, aún no se encuentra comercializado, por lo que no es posible analizar su costo-efectividad en este momento.
CONCLUSIONES
Los inhibidores de miosina han demostrado ser una opción segura y eficaz en el tratamiento de la MCHO, posicionándose actualmente como una alternativa de segunda línea. Sin embargo, aún se necesita más evidencia para considerarlos de primera línea, especialmente en términos de su impacto estructural y su efecto en eventos clínicos duros a largo plazo, como mortalidad, arritmias y necesidad de dispositivos. Su potencial para modular la evolución de la enfermedad es un aspecto clave a investigar, particularmente en relación con la regresión de la hipertrofia y la reducción de la fibrosis miocárdica.
Por otro lado, su alto costo y la dificultad de acceso en muchos sistemas de salud, incluido el nuestro, limitan su disponibilidad y subrayan la importancia de una selección cuidadosa de los pacientes que más pueden beneficiarse. A pesar de estos desafíos, su uso en formas no obstructivas y en pacientes asintomáticos resulta promisorio, abriendo nuevas perspectivas en el manejo y en la posible modificación del curso natural de la MCH.
Declaración de conflicto de Intereses
Los autores declaran que no tienen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la Web).